题目内容
6.一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示.下列判断正确的是( )
| A. | 在0-50min之间,pH=2和pH=7时R的降解百分率不相等 | |
| B. | 溶液酸性越强,R的降解速率越小 | |
| C. | R的起始浓度和溶液的pH均影响R的降解速率 | |
| D. | 在 20-25min之间,pH=10 时R的平均降解速率为 0.04mol•L-1•min-1 |
分析 A.根据图中的信息可以知道在0-50min之间,pH=2和pH=7时R的降解百分率;
B.对比溶液的酸性强弱对R的降解速率的影响情况;
C.根据题中给出的曲线变化判断;
D.根据平均降解速率v=$\frac{△c}{△t}$来计算即可.
解答 解:A.根据图示可知:在0-50min之间,pH=2和pH=7时R的降解百分率都为100%,故A错误;
B.溶液酸性越强,即pH越小,线的斜率越大,可以知道R的降解速率越大,故B错误;
C.根据图中曲线可知,曲线的斜率表示反应速率,起始浓度不同分解速率不同,PH不同分解速率也不同,故R的起始浓度和溶液的PH均影响R的降解速率,故C正确;
D.在 20-25min之间,pH=10时R的平均降解速率为:$\frac{0.6-0.4}{5}$=0.04×10-4mol•L-1•min-1,故D错误;
故选C.
点评 本题考查了化学平衡的影响因素,题目难度中等,明确图象曲线变化的含义为解答关键,注意掌握外界条件对化学平衡、化学反应速率的影响,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
14.某同学用某种粗盐进行提纯实验,步骤见下图.
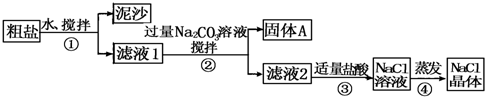
请回答:
(1)步骤①和②的操作名称是过滤.
(2)步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止液体溅出,当蒸发皿中有较多量固体出现时,应停止加热,用余热使水分蒸干.
(3)猜想和验证:

请回答:
(1)步骤①和②的操作名称是过滤.
(2)步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止液体溅出,当蒸发皿中有较多量固体出现时,应停止加热,用余热使水分蒸干.
(3)猜想和验证:
| 猜想 | 验证的方法 | 现象 | 结论 |
| 猜想Ⅰ:固体A中含CaCO3、MgCO3 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 | 有气泡冒出且烧杯中产生白色沉淀 | 猜想Ⅰ成立 |
| 猜想Ⅱ:固体A中含BaCO3 | 取少量固体A于试管中,先滴入稀盐酸或稀硝酸,再滴入Na2SO4溶液 | 有气泡放出,无白色沉淀 | 猜想II不成立 |
| 猜想Ⅲ:最后制得的NaCl晶体中还含有Na2SO4 | 取少量NaCl晶体溶于试管中的蒸馏水,加入硝酸酸化的硝酸钡溶液 | 产生不溶于稀硝酸的白色沉淀 | 猜想Ⅲ成立 |
1.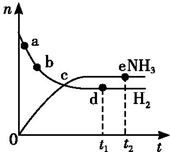 向绝热恒容密闭容器中通入N2和H2,在一定条件下使反应N2(g)+3H2(g)?2NH3(g)△H<0达到平衡,n(H2)和n(NH3)随时间变化的关系如图所示.下列有关叙述一定正确的是( )
向绝热恒容密闭容器中通入N2和H2,在一定条件下使反应N2(g)+3H2(g)?2NH3(g)△H<0达到平衡,n(H2)和n(NH3)随时间变化的关系如图所示.下列有关叙述一定正确的是( )
 向绝热恒容密闭容器中通入N2和H2,在一定条件下使反应N2(g)+3H2(g)?2NH3(g)△H<0达到平衡,n(H2)和n(NH3)随时间变化的关系如图所示.下列有关叙述一定正确的是( )
向绝热恒容密闭容器中通入N2和H2,在一定条件下使反应N2(g)+3H2(g)?2NH3(g)△H<0达到平衡,n(H2)和n(NH3)随时间变化的关系如图所示.下列有关叙述一定正确的是( )| A. | c点表示NH3生成速率与NH3分解速率相等 | |
| B. | c点和e点H2的转化率相等 | |
| C. | 平衡后再升高温度,不利于氨的合成 | |
| D. | d点时:n(H2):n(NH3)=3:2 |
15.在一定温度下,向一个容积固定的密闭真空容器中充入2molX气体,发生反应X(g)?Y(g)+Z(g),使反应达到平衡,这时容器中的混合气体中X气体的体积分数是a%.若在同一容器中,最初放入的是1molY和1molZ的混合气体,并在相同的温度下使反应达到平衡,这时混合气体中X 气体所占的体积分欲是b%.则a和b的关系是( )
| A. | a>b | B. | a=b | C. | a<b | D. | 2a=b |
16.下列过程中△H小于零的是( )
| A. | 氯酸钾分解制氧气 | B. | 氯化铵分解得氨气 | ||
| C. | 碳酸钙分解得二氧化碳 | D. | 实验室制备氢气 |


