题目内容
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:下列说法错误的是( )
| 物质 | X | Y | Z |
| 初始浓度/mol?L-1 | 0.1 | 0.2 | 0 |
| 2min后平衡浓度/mol?L-1 | 0.05 | 0.05 | 0.1 |
| A、反应达到平衡时,X的转化率为50% |
| B、反应可表示为X+3Y?2Z,其平衡常数为1600 |
| C、改变温度可以改变此反应的平衡常数 |
| D、用Y来表示的该反应的反应速率为0.025 mol?L-1min-1 |
考点:化学平衡的计算
专题:化学平衡专题
分析:A.根据转化率=
计算;
B.根据反应速率之比等于化学计量数之比判断化学方程式并计算平衡常数;
C.平衡常数只受温度的影响;
D.根据V=
进行计算.
| 转化量 |
| 初始量 |
B.根据反应速率之比等于化学计量数之比判断化学方程式并计算平衡常数;
C.平衡常数只受温度的影响;
D.根据V=
| △c |
| △t |
解答:
解:A.反应达到平衡时,X的转化率为:
=50%,故A正确;
B.根据反应速率之比等于浓度变化量之比等于化学计量数之比可知:△c(X):△c(Y):△c(Z):=0.05:0.15:0.1=1:3:2,则反应的方程式为X+3Y?2Z,K=
=
=1600(mol/L)-2,故B正确;
C.平衡常数只受温度的影响,温度改变时,化学平衡常数一定变化,故C正确;
D.用Y来表示的该反应的反应速率为
=0.075 mol?L-1min-1,故D错误;
故选D.
| 0.1mol/L-0.05mol/L |
| 0.1mol/L |
B.根据反应速率之比等于浓度变化量之比等于化学计量数之比可知:△c(X):△c(Y):△c(Z):=0.05:0.15:0.1=1:3:2,则反应的方程式为X+3Y?2Z,K=
| c 2(Z) |
| c(X)?c 3(Y) |
| (0.1mol/L)2 |
| (0.05mol/L)×(0.05mol/L)3 |
C.平衡常数只受温度的影响,温度改变时,化学平衡常数一定变化,故C正确;
D.用Y来表示的该反应的反应速率为
| 0.2-0.05 |
| 2 |
故选D.
点评:本题考查化学平衡的计算及平衡移动问题,题目难度不大,注意平衡常数的计算以及平衡常数为温度的函数的特征来解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
乙烯制聚乙烯,所发生的反应属于( )
| A、加成反应 | B、加聚反应 |
| C、取代反应 | D、酯化反应 |
 豪猪烯(hericenes),形状宛如伏地伸刺的动物,其键线式如图.豪猪烯(hericenes),形状宛如伏地伸刺的动物,其键线式如右图.下列有关豪猪烯的说法正确的是( )
豪猪烯(hericenes),形状宛如伏地伸刺的动物,其键线式如图.豪猪烯(hericenes),形状宛如伏地伸刺的动物,其键线式如右图.下列有关豪猪烯的说法正确的是( )| A、豪猪烯与乙烯互为同系物 |
| B、豪猪烯分子中所有原子在同一平面 |
| C、豪猪烯的分子式为:C14H20 |
| D、豪猪烯能使酸性高锰酸钾溶液褪色 |
下列有关物质的表达式不正确的是( )
| A、二甲醚的分子式:C2H6O |
B、COCl2分子的结构式: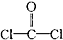 |
| C、醛基的结构简式:-CHO |
D、溴乙烷的电子式: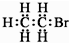 |
浅绿色的Fe(NO3)2溶液中存在平衡:Fe2++2H2O?Fe(OH)2+2H+,若向溶液中加入稀盐酸,则溶液的颜色( )
| A、绿色变浅 | B、绿色变深 |
| C、变黄 | D、不变 |
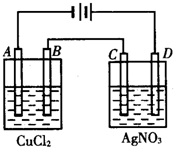 如图为以惰性电极进行电解.完成下列问题
如图为以惰性电极进行电解.完成下列问题