题目内容
3.X、Y、Z、W是原子序数依次增大的四种短周期主族元素.Y、Z同周期且相邻,X、W同主族且与Y处于不同周期,Y、Z原子的电子数总和与X、W原子的电子数总和之比为5:4.下列说法正确的是( )| A. | 化合物WY3中只含有离子键 | |
| B. | Y的简单气态氢化物的沸点比Z的低 | |
| C. | 原子半径:r(W)>r(Z)>r(Y)>r(X) | |
| D. | 由X、Z组成的化合物与由Z、W组成的化合物只能发生化合反应 |
分析 X、Y、Z、W是原子序数依次增大的短周期元素,X、W同主族且与Y处于不同周期,则X为H元素、W为Na元素;Y、Z同周期且相邻,且不与X、W不同周期,则二者位于第二周期,Y、Z原子的电子数总和与X、W原子的电子数总和之比为5:4,设Y的原子序数为x,则Z的原子序数为x+1,则:$\frac{x+x+1}{1+11}$=$\frac{5}{4}$,解得:x=7,则Y为N元素、Z为O元素,以此解答该题.
解答 解:由上述分析可知,X为H,Y为N,Z为O,W为Na,
A.化合物WY3为NaN3,含离子键及N、N之间的共价键,为离子化合物,故A错误;
B.水中氢键数目多,则Y的简单气态氢化物的沸点比Z的低,故B正确;
C.电子层越多,原子半径越大,电子层相同时,核电荷数越大,原子半径越小,则原子半径大小为:r(W)>r(Y)>r(Z)>r(X),故C错误;
D.由X、Z组成的化合物为水时,与由Z、W组成的化合物过氧化钠发生氧化还原反应生成氧气,故D错误;
故选B.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、电子数关系来推断元素为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
13.仅用下表提供的实验用品(规格、数量不限),能实现相应实验目的是( )
| 选项 | 实验用品(省略夹持装置) | 相应实验 |
| A | 蒸发皿、玻璃棒、泥三角、三脚架 | 从食盐水中获得NaCl晶体 |
| B | 烧杯、玻璃棒、漏斗、滤纸 | 除去氢氧化铝胶体中的泥沙 |
| C | 烧杯、玻璃棒、胶头滴管、容量瓶 | 用胆矾配制100mL0.1mol/L的硫酸铜溶液 |
| D | 蒸馏烧瓶、温度计、冷凝管、石棉网、牛角管、锥形瓶、酒精灯 | 用四氯化碳萃取溴水中的溴 |
| A. | A | B. | B | C. | C | D. | D |
14.将2.56g Cu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12L(标准状况),则反应过程中转移的电子为( )
| A. | 0.08 mol | B. | 0.16 mol | C. | 0.24 mol | D. | 0.32mol |
11.仅用下表提供的仪器(夹持仪器和试剂任选),能实现相应实验目的是( )
| 选项 | 实验目的 | 仪器 |
| A | 硫酸铜溶液的浓缩结晶 | 坩埚、玻璃棒、烧杯 |
| B | 用稀H2SO4、Na2CO3溶液比较元素S与C的非金属强弱 | 试管、胶头滴管 |
| C | 用8.0mol•L-1的盐酸配制250mL 1.5mol•L-1 的盐酸 | 250mL容量瓶,玻璃棒、烧杯 |
| D | 测定NaOH溶液的物质的量浓度 | 酸(碱)式滴定管,胶头滴管、烧杯 |
| A. | A | B. | B | C. | C | D. | D |
18.能证明KOH是离子化合物的事实是( )
| A. | 常温下是固体 | B. | 易溶于水 | C. | 水溶液能导电 | D. | 熔融态能导电 |
8.下列实验设计正确的是( )
| A. | 检验淀粉已完全水解;在淀粉水解液中滴加碘水 | |
| B. | 证明氧化性H2O2比Fe3+强,将硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中 | |
| C. | 检验某溶液中含Fe2+:可先向溶液中加入氯气,再滴加少量KSCN溶液 | |
| D. | 把0.9mol•L-1硫酸100mL;将18 mol•L-1硫酸5mL移入100mL容量瓶,加水至刻度 |
4.下列叙述错误的是( )
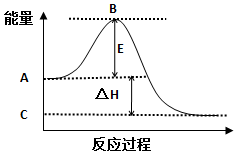
| A. | 过程的自发性只能用于判断过程的方向性,不能确定过程是否一定会发生和过程发生的速率 | |
| B. | 空气污染日报中的空气污染指数的主要项日有可吸入颗粒物、二氧化硫、二氧化氮 | |
| C. | 金属冶炼过程主要是利用金属矿物中的金属离子失去电子变成金属单质所发生的氧化还原反应 | |
| D. | 糖类和油脂是重要的基本营养物质,并且是人体所需能量的重要来源 |
5.CuBr是一种白色晶体,见光或潮湿时受热易分解,在空气中逐渐变为浅绿色.实验室制备CuBr的反应原理为SO2+2CuSO4+2NaBr+2H2O═2CuBr↓+2H2SO4+Na2SO4,用下列装置进行实验,不能达到实验目的是( )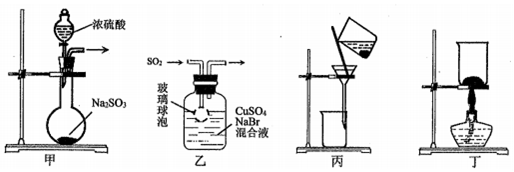

| A. | 用装置甲制取SO2 | B. | 用装置乙制取CuBr | ||
| C. | 用装置丙避光将CuBr与母液分离 | D. | 用装置丁干燥CuBr |