题目内容
16.NA代表阿伏加德罗常数,下列说法正确的是( )| A. | 常温常压下,2.24LC2H4和C2H2的混合气体中含碳原子数目小于0.2NA | |
| B. | 100mL1.0mol/L的FeCl3溶液与足量Cu反应,转移电子数数为0.2NA | |
| C. | 标况下44.8mL氯气通入足量水中发生反应,转移电子数为2×10-3NA | |
| D. | 常温下,pH=2的H2SO4溶液中含有的H+数目为0.02NA |
分析 A.常温常压下,气体摩尔体积大于22.4L/mol;
B.根据n=cV计算出铁离子的物质的量,然后计算出转移电子的物质的量及数目;
C.氯气与水的反应为可逆反应,则氯气不会完全反应;
D.缺少溶液体积,无法计算溶液中氢离子的数目.
解答 解:A.常温常压下,气体摩尔体积大于22.4L/mol,则2.24LC2H4和C2H2的混合气体的物质的量小于$\frac{2.24L}{22.4L/mol}$=0.1mol,则混合气体中含碳原子数目小于0.2NA,故A正确;
B.100mL1.0mol/L的FeCl3溶液中含有氯化铁的物质的量为0.1mol,0.1mol氯化铁与足量Cu反应转移了0.1mol电子,转移电子数数为0.1NA,故B错误;
C.只有部分氯气与水反应,则无法计算转移的电子数,故C错误;
D.没有告诉溶液体积,无法计算溶液中氢离子的物质的量及数目,故D错误;
故选A.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
6.通过α粒子轰击金箔的实验现象,否定葡萄干面包原子模型的科学家是( )
| A. | 伦琴 | B. | 卢瑟福 | C. | 道尔顿 | D. | 汤姆孙 |
7.10.0g某有机物在氧气中充分燃烧生成CO2和H2O,将这些燃烧产物与足量Na2O2充分反应,Na2O2能增重10.0g,此有机物不可能是( )
| A. | C6H12O6 | B. | C2H5OH | C. | HCHO | D. | CH3COOH |
4.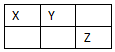 X、Y、Z、W是元素周期表前四周期元素,X、Y、Z是短周期元素,它们在周期表中的位置关系如图所示,其中Y原子的最外层电子数是电子层数的3倍.W的原子总数是Z的2倍.下列说法不正确的是( )
X、Y、Z、W是元素周期表前四周期元素,X、Y、Z是短周期元素,它们在周期表中的位置关系如图所示,其中Y原子的最外层电子数是电子层数的3倍.W的原子总数是Z的2倍.下列说法不正确的是( )
 X、Y、Z、W是元素周期表前四周期元素,X、Y、Z是短周期元素,它们在周期表中的位置关系如图所示,其中Y原子的最外层电子数是电子层数的3倍.W的原子总数是Z的2倍.下列说法不正确的是( )
X、Y、Z、W是元素周期表前四周期元素,X、Y、Z是短周期元素,它们在周期表中的位置关系如图所示,其中Y原子的最外层电子数是电子层数的3倍.W的原子总数是Z的2倍.下列说法不正确的是( )| A. | W位于元素周期表第四周期ⅥA族 | |
| B. | X、W、Z的最高正化合价依次升高 | |
| C. | X、Y、Z三种元素都能与氢形成18电子化合物 | |
| D. | 简单离子半径:W>Y>X>Z |
19.下列装置或操作能达到实验目的是( )
| A. | 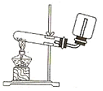 实验室制取并收集NH3 | B. | 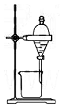 用乙醇提取溴水中的溴 | ||
| C. | 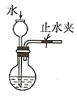 检查装置气密性 | D. | 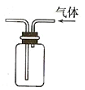 利用排空气法收集CO |