题目内容
11.一定温度下若要使NH4Cl溶液中c(NH4+)/c(Cl-)比值增大,可采取的方法是( )| A. | 加少量水 | B. | 加少量NaOH固体 | C. | 加少量浓氨水 | D. | 通入少量HCl气体 |
分析 在氯化铵溶液中存在以下平衡:NH4++H2O?NH3•H2O+H+,要使c(NH4+)/c(Cl-)的值增大,即NH4+的浓度增大,则平衡逆移或者加入NH4+的条件均可以,以此解答该题.
解答 解:A.加水,促进了铵根离子的水解,平衡右移,n(NH4+)减小,n(Cl-)不变,且二者比值等于c(NH4+)/c(Cl-),应减小,故A错误;
B.加入NaOH固体,与NH4+反应,则c(NH4+)/c(Cl-)比值减小,故B错误;
C.加少量浓氨水,抑制了铵根离子的水解,NH4+的浓度增大,而且NH3•H2O能部分电离生成NH4+,c(NH4+)/c(Cl-)比值增大,故正确;
D.通入氯化氢气体,溶液中c(Cl-)增大,同时平衡逆移c(NH4+)增大,由于平衡移动引起的浓度变化比较小,所以溶液中c(Cl-)增大的程度比c(NH4+)增大的程度大,c(NH4+)/c(Cl-)比值减小,故D错误.
故选C.
点评 本题考查盐类水解平衡的移动原理,为高频考点,侧重考查学生的分析能力,题目难度不大,注意把握影响水解平衡移动的因素是解题关键.

练习册系列答案
相关题目
1.在密闭容器中,放入镍粉并充入一定量CO气体,一定条件下发生反应:Ni(s)+4CO(g)?Ni(CO)4(g),已知该反应在25℃和80℃时的平衡常数分别为5×104和2,下列说法正确的是( )
| A. | 上述生成Ni(CO)4(g)的反应为吸热反应 | |
| B. | 恒温恒压下,向容器中再充入少量的Ar,上述平衡将正向移动 | |
| C. | 在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5 mol/L,则此时v正<v逆 | |
| D. | 恒温恒容下,向容器中再充入少量Ni(CO)4(g),达新平衡时,CO 的百分含量将增大 |
2.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 使甲基橙变红的溶液中:Na+、Cl-、CH3 COO-、Fe2+ | |
| B. | 加铝粉能产生大量H2的溶液中:Na+、NH4+、NO3-、Cl- | |
| C. | 无色溶液中:Al3+、NO3-、Cl-、SO42- | |
| D. | c(FeCl3)=1.0mol/L的溶液中:HCO3-、Cl-、H+、Na+ |
19.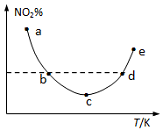 取5等份(各1mol)NO2,分别加入温度不同的2L恒容密闭容器中,发生反应:2NO2(g)?N2O4(g).反应10s时,分别测定体系中NO2的百分含量(NO2%),并作出其随反应温度(T)变化的关系图.据图分析,下列说法正确的是( )
取5等份(各1mol)NO2,分别加入温度不同的2L恒容密闭容器中,发生反应:2NO2(g)?N2O4(g).反应10s时,分别测定体系中NO2的百分含量(NO2%),并作出其随反应温度(T)变化的关系图.据图分析,下列说法正确的是( )
 取5等份(各1mol)NO2,分别加入温度不同的2L恒容密闭容器中,发生反应:2NO2(g)?N2O4(g).反应10s时,分别测定体系中NO2的百分含量(NO2%),并作出其随反应温度(T)变化的关系图.据图分析,下列说法正确的是( )
取5等份(各1mol)NO2,分别加入温度不同的2L恒容密闭容器中,发生反应:2NO2(g)?N2O4(g).反应10s时,分别测定体系中NO2的百分含量(NO2%),并作出其随反应温度(T)变化的关系图.据图分析,下列说法正确的是( )| A. | 图中a、b两点对应的反应未达到平衡状态 | |
| B. | 图中b、d两点对应的NO2速率相等 | |
| C. | 该反应为吸热反应 | |
| D. | e点对应的容器中气体颜色最深 |
16.已知25℃时有关弱酸的电离平衡常数如表:下列推断正确的是( )
| 弱酸化学式 | HX | HY | H2CO3 |
| 电离平衡常数 | 7.8×10-9 | 3.7×10-15 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | pH相同的HX、HY溶液,HY的物质的量浓度小 | |
| B. | 相同条件下溶液的碱性:NaX>Na2CO3>NaY>NaHCO3 | |
| C. | 结合H+的能力:Y->CO32->X->HCO3- | |
| D. | 向NaX溶液中通入CO2的化学方程式:2NaX+CO2+H2O=Na2CO3+2HX |
3.X、Y、Z、W、R是5种短周期元素,其原子序数依次增大.X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等.下列说法不正确的是( )
| A. | W、Y、R的简单离子半径依次增大 | |
| B. | X、R、Z都可与Y形成两种化合物 | |
| C. | X2Y的热稳定性强于X2R、沸点也高于X2R,但解释的理由不相同 | |
| D. | Z元素分别与X元素和Y元素形成的化合物都是离子晶体,均能与水反应且一定生成了强碱和无色气体 |
20.下列关于氯气的叙述正确的是( )
| A. | 钠在氯气中燃烧产生白色烟雾 | |
| B. | 红热的铜丝可以在氯气中燃烧,产生棕黄色烟雾 | |
| C. | 纯净的氢气可以在氯气中安静地燃烧,发出苍白色火焰 | |
| D. | 氯气可用于漂白,这是氯气的漂白作用 |
1.下列关于油脂的叙述正确的是( )
| A. | 油脂均为固体 | |
| B. | 油脂在体内直接氧化产生热量 | |
| C. | 多吃动物脂肪比多吃植物油有利 | |
| D. | 有些脂肪酸是人体必需的,但在人体内却不能合成;脂肪中必需脂肪酸的含量越高,其营养价值越高 |
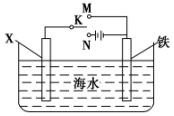 利用如图装置,可以模拟铁的电化学防护.
利用如图装置,可以模拟铁的电化学防护.