题目内容
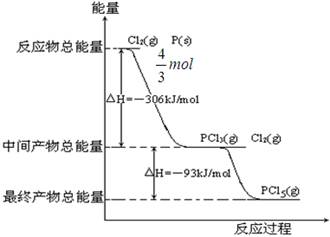
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
根据右图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式__________________________________。
(2)PCl5分解成PCl3和Cl2的热化学方程式_________________________________,上述分解反应是一个可逆反应,温度T1时,在密闭容器中加入0.80molPCl5,反应达到平衡时PCl5还剩0.60mol,其分解率α1等于___________;若反应温度由T1升高到T2,平衡时PCl5的分解率为α2,α2_____α1(填“大于”、“小于”或“等于”)。
(3)工业上制备PCl5通常分两步进行,先将P和Cl2反应生成中间产物PCl3,然后降温,再和Cl2反应生成PCl5。原因是________________________________________________。
(4)P和Cl2分两步反应生成1molPCl5的△H3=______________________,P和Cl2一步反应生成1molPCl5的△H4___________△H3(填“大于”、“小于”或“等于”)。
(1)P(s)+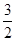 Cl2(g)
Cl2(g) PCl3(g) △H=-306kJ/mol
PCl3(g) △H=-306kJ/mol
(2)PCl5(g) PCl3(g)+Cl2(g) △H=+93kJ/mol 25% 大于
PCl3(g)+Cl2(g) △H=+93kJ/mol 25% 大于
(3)两步反应均为放热反应,降温有利于提高产率,防止产物分解
(4)等于
【解析】
试题分析:(1)根据图像可知,1molP在Cl2中完全燃烧放出的热量为306kJ•mol-1,所以P与Cl2反应生成PCl3的热化学反应方程式为P(s)+32Cl2(g)=PCl3(g) △H=-306kJ•mol-1。
(2)中间产物PCl3和未完全反应的Cl2的总能量高于最终产物PCl5的能量,其△H=-93kJ•mol-1,所以PCl5(g)=PCl3(g)+Cl2(g);△H=93kJ•mol-1;分解率α1=(0.80mol-0.60mol)/0.80mol×100%=25%。由热化学反应方程式可知,此反应的正反应为吸热反应,所以升高温度,平衡向正反应方向移动,PCl5的分解率增大。即:α2>α1。
(3)根据图像可知,P与Cl2反应生成PCl3,PCl3和Cl2进一步反应生成PCl5,都是放热反应,分两步进行且第二步降低温度,有利于PCl5的生成,防止PCl5的分解。
(4)由盖斯定律可知,一步生成生成PCl5和两步生成PCl5的总的热效应相等,所以△H3=-306kJ/mol-93kJ/mol=-399kJ•mol-1。
考点:考查热化学方程式的书写、盖斯定律的应用及有关计算等
点评:本题为2008全国2试卷试题的前4问,属于中等难度的试题,试题基础性强。根据图示分析反应物与生成物的能量大小关系,即可以完成相关解答。

 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。


