题目内容
16.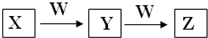 X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图转化关系:
X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图转化关系:(1)若该反应是非氧化还原反应
①X为强碱溶液,W是形成酸雨的主要气体,则Y到Z的离子方程式为SO32-+SO2+H2O=2HSO3-
②X是一种盐,焰色反应为黄色,逐滴加入W,溶液中开始无气泡,后产生无色无味气体Z,Y的化学式为NaHCO3.
③若W为一种强碱,Y具有两性,则向Z溶液中通入少量二氧化碳的离子方程式为2AlO2-+CO2+3H2O=2Al(OH)3+CO32-.
(2)若该反应是氧化还原反应
①X常温下为黄绿色气体,W是生活中应用最广泛的金属之一,则Y的水溶液中加入W生成Z溶液的离子方程式为2Fe3++Fe=3Fe2+.
②X常温下为气体化合物,Z是一种红棕色气体,X气体的检验方法湿润的红色石蕊试纸若变蓝或遇蘸有浓盐酸的玻璃棒产生白烟,X转化为Y的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
分析 (1)①X为强碱溶液,W是形成酸雨的主要气体,W为SO2,Y、Z分别含有SO32-、HSO3-;
②X是一种盐,焰色反应为黄色,则X为钠盐,逐滴加入W,溶液中开始无气泡,后产生无色无味气体Z,Z为CO2,则X为Na2CO3,Y为NaHCO3,W为酸;
③若W为一种强碱,Y具有两性,则X为铝盐,Y为Al(OH)3,Z为偏铝酸盐;
(2)①X常温下为黄绿色气体,则X为Cl2,W是生活中应用最广泛的金属之一,由转化关系可知应为变价金属,则W为Fe,Y为FeCl3、Z为FeCl2;
②X常温下为气体化合物,Z是一种红棕色气体,则Z为NO2,X为NH3,W为O2,Y为NO.
解答 解:(1)①X为强碱溶液,W是形成酸雨的主要气体,W为SO2,Y、Z分别含有SO32-、HSO3-,则Y到Z的离子方程式为:SO32-+SO2+H2O=2HSO3-,
故答案为:SO32-+SO2+H2O=2HSO3-;
②X是一种盐,焰色反应为黄色,则X为钠盐,逐滴加入W,溶液中开始无气泡,后产生无色无味气体Z,Z为CO2,则X为Na2CO3,Y为NaHCO3,W为酸.
故答案为:NaHCO3;
③若W为一种强碱,Y具有两性,则X为铝盐,Y为Al(OH)3,Z为偏铝酸盐,向Z溶液中通入少量二氧化碳的离子方程式为:2AlO2-+CO2+3H2O=2Al(OH)3+CO32-,
故答案为:2AlO2-+CO2+3H2O=2Al(OH)3+CO32-;
(2)①X常温下为黄绿色气体,则X为Cl2,W是生活中应用最广泛的金属之一,由转化关系可知应为变价金属,则W为Fe,Y为FeCl3、Z为FeCl2,Y的水溶液中加入W生成Z溶液的离子方程式为:2Fe3++Fe=3Fe2+,
故答案为:2Fe3++Fe=3Fe2+;
②X常温下为气体化合物,Z是一种红棕色气体,则Z为NO2,X为NH3,W为O2,Y为NO,NH3的检验方法:湿润的红色石蕊试纸若变蓝或遇蘸有浓盐酸的玻璃棒产生白烟,NH3转化为NO的化学方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:湿润的红色石蕊试纸若变蓝或遇蘸有浓盐酸的玻璃棒产生白烟;4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
点评 本题考查无机物的推断,注意根据物质的颜色、性质结合转化关系推断,熟练中学中学常见的连续反应,题目难度中等.

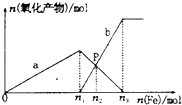 向含有1mol HNO3和1mol H2SO4的混合溶液中逐渐加人铁粉至过量溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO).下列有关判断不正确的是( )
向含有1mol HNO3和1mol H2SO4的混合溶液中逐渐加人铁粉至过量溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO).下列有关判断不正确的是( )| A. | a表示Fe3+的关系曲线,b表示Fe3+的关系曲线 | |
| B. | P点时,n(Fe3+)=0.50 mol | |
| C. | n1=0.75 | |
| D. | n1:n3=2:3 |
| A. | 空气中电子式为${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{C}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$的分子含量过多会造成温室效应 | |
| B. | 结构示意图为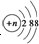 的阴离子都不能破坏水的电离平衡 的阴离子都不能破坏水的电离平衡 | |
| C. | 球棍模型为 的分子可发生加成反应 的分子可发生加成反应 | |
| D. | 电子式分别为Na+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$]2-Na+和H${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$H的两种化合物均为常见的氧化剂 |
| A. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+2H2O+4NH4+ | |
| B. | 过量铁粉溶于稀硝酸:Fe+NO3-+4H+═Fe3++2H2O+NO↑ | |
| C. | 氯气与水的反应:H2O+Cl2═2H++Cl-+ClO- | |
| D. | 向明矾溶液中滴加Ba(OH)2溶液,使沉淀物质的量最大:2Al3++3 Ba2++3SO42-+6OH-═2Al(OH)3↓+3BaSO4↓ |
| A. | SO2有漂白性,所以能使滴有酚酞的NaOH溶液褪色 | |
| B. | SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,其原理相同 | |
| C. | 能使品红溶液褪色的不一定是SO2 | |
| D. | SO2和Cl2都能漂白,若将两种气体同时通入,漂白效果会更好 |
| A. | 平衡向正反应方向移动了 | B. | 物质A的转化率减少了 | ||
| C. | 物质B的质量分数增加了 | D. | a<b+c |

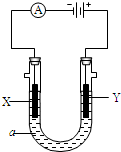 电解原理在化学工业中有广泛应用,如图为工业制氯气的装置原理.U型管中装有电解液a;X、Y是两根电极棒,通过导线与直流电源相连,实验开始时,同时在两边各滴入几滴酚酞试液.请回答以下问题:
电解原理在化学工业中有广泛应用,如图为工业制氯气的装置原理.U型管中装有电解液a;X、Y是两根电极棒,通过导线与直流电源相连,实验开始时,同时在两边各滴入几滴酚酞试液.请回答以下问题: