��Ŀ����
һ�������£����ݻ�Ϊ10L���ܱ������У���l mol X��1mol Y�������·�Ӧ��2X��g��+Y��g��?Z��g������60s�ﵽƽ������0.3mol��Z������˵����ȷ���ǣ�������
| A��60 s��X��ƽ����Ӧ����Ϊ0.01 mol?L-1?s-1 |
| B�������¶ȣ���X�����������С��������Ӧ�ġ�H��0 |
| C�����������ݻ���Ϊ20 L����ƽ���Z��Ũ��Ϊ0.015 mol?L-1 |
| D�������¶Ⱥ�������䣬���ٳ���1 mol X��Y��ת���ʽ����� |
���㣺��ѧƽ��ļ���
ר�⣺
������һ�������£����ݻ�Ϊ10L���ܱ������У���1molX��1molY�������·�Ӧ��2X��g��+Y��g��?Z��g������60s�ﵽƽ������0.3mol��Z������ƽ������ʽ��ʽ�õ�
2X��g��+Y��g��?Z��g��
��ʼ����mol�� 1 1 0
�仯����mol�� 0.6 0.3 0.3
ƽ������mol�� 0.4 0.7 0.3
���ݼ���������ѡ�
2X��g��+Y��g��?Z��g��
��ʼ����mol�� 1 1 0
�仯����mol�� 0.6 0.3 0.3
ƽ������mol�� 0.4 0.7 0.3
���ݼ���������ѡ�
���
�⣺һ�������£����ݻ�Ϊ10L���ܱ������У���1molX��1molY�������·�Ӧ��2X��g��+Y��g��?Z��g������60s�ﵽƽ������0.3mol��Z����
2X��g��+Y��g��?Z��g��
��ʼ����mol�� 1 1 0
�仯����mol�� 0.6 0.3 0.3
ƽ������mol�� 0.4 0.7 0.3
A��60sʱX��ƽ����Ӧ����Ϊ=
=0.001mol?L-1?s-1����A����
B���������¶ȣ�X�����������С��˵��ƽ��������У�����Ӧ�����ȷ�Ӧ����Ӧ�ġ�H��0����B����
C���������ݻ���Ϊ20L��������ƽ���ƶ���Z����ƽ��Ũ�Ƚ�����ԭƽ��Ũ�ȵ�һ�룬ѹǿ��С��ƽ��������У�Z��Ũ�ȴ���ԭ����һ�룬��C����
D�����¶Ⱥ�������䣬������������1molX��ƽ��������У�Y��ת���ʽ�����D��ȷ��
��ѡ��D��
2X��g��+Y��g��?Z��g��
��ʼ����mol�� 1 1 0
�仯����mol�� 0.6 0.3 0.3
ƽ������mol�� 0.4 0.7 0.3
A��60sʱX��ƽ����Ӧ����Ϊ=
| ||
| 60 |
B���������¶ȣ�X�����������С��˵��ƽ��������У�����Ӧ�����ȷ�Ӧ����Ӧ�ġ�H��0����B����
C���������ݻ���Ϊ20L��������ƽ���ƶ���Z����ƽ��Ũ�Ƚ�����ԭƽ��Ũ�ȵ�һ�룬ѹǿ��С��ƽ��������У�Z��Ũ�ȴ���ԭ����һ�룬��C����
D�����¶Ⱥ�������䣬������������1molX��ƽ��������У�Y��ת���ʽ�����D��ȷ��
��ѡ��D��
���������⿼���˻�ѧƽ�������ʽ����Ӧ�ã�ƽ��Ӱ�����صķ����жϣ�ƽ���ƶ�ԭ���������ǽ���ؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
��0.05molBa��OH��2����ֱ���뵽����100mLҺ���У���Һ�����Ի������䣮��Һ���ǣ�������
| A��1.0mol/L���� |
| B������ˮ |
| C��0.5mol/L���� |
| D��1.0mol/L��ˮ |
ij�¶��£����������������н��з�Ӧ��CO��g��+2H2��g��?CH3OH��g����H1=-90.7kJ?mol-1����֪��Ӧ����ʼŨ�ȷֱ�Ϊ��c��CO��=1mol/L��c��H2��=2.4mol/L��5min��Ӧ��ƽ�⣬��ʱCO��ת����Ϊ50%��������˵����ȷ���ǣ�������
| A���÷�Ӧ�����������ȷ�Ӧ��һ�����Է����� |
| B��5 min��H2��ƽ����Ӧ����Ϊ0.1 mol/��L?min�� |
| C�������������������£�������������CO��ת���� |
| D�������¶��£���Ӧ�����ʼŨ��c��CO��=4 mol/L��c��H2��=a mol/L���ﵽƽ���c��CH3OH��=2 mol/L����a=5.4 |
����ʵ��������д�����ǣ�������
| A������ʱ������ˮӦ�������ܵ��¿�ͨ�롢�Ͽ������ҽ��¶ȼ�ˮ�������Һ���� |
| B����Һʱ����Һ©���²�Һ����¿ڷų����ϲ�Һ��Ҳ���¿ڷų� |
| C����ȡʱ����ȡ����ѡȡ���ܶ��� |
| D������ʱ������Һ�г�����������Ӧֹͣ���ȣ�������������ʣ����Һ |
���������У����ܷ�����ȥ��Ӧ����ϩ�������ܷ���������Ӧ����ȩ���ǣ�������
| A���״� |
| B��2-��-2-���� |
| C��2-��-1-���� |
| D��2-���� |
ƻ���п���������ڿ����л�ܿ��ƣ����˳�֮Ϊ��ƻ�����⡱������ά����C��ҺͿ�����п��������ϣ�����Ͳ���Ѹ�ٱ�ɻ�ɫ����˵��ά����C���У�������
| A�������� | B����ԭ�� |
| C������ | D������ |
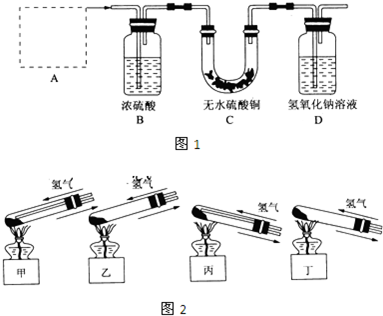
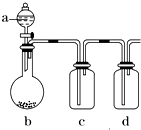 �м���ʵ��С���ͬѧ��������ͼװ�ý��С�һ�����á���ʵ��̽����a��ʢ�ŵ�Һ��������ٵ��£�b��ʢ�ŵ�ҩƷ����������c��d��ʢװҺ�壬���ܾ�����Һ�����£���ÿ��ͬѧ������a��b��c��d�зֱ�ʢ�Ų�ͬ���ʣ�����ȡij�����岢���������ʣ�
�м���ʵ��С���ͬѧ��������ͼװ�ý��С�һ�����á���ʵ��̽����a��ʢ�ŵ�Һ��������ٵ��£�b��ʢ�ŵ�ҩƷ����������c��d��ʢװҺ�壬���ܾ�����Һ�����£���ÿ��ͬѧ������a��b��c��d�зֱ�ʢ�Ų�ͬ���ʣ�����ȡij�����岢���������ʣ�