题目内容
3.下列各组中的两种物质作用时,反应条件或反应物用量改变时,对生成物没有影响的是( )| A. | Na2O2与CO2 | B. | Na与O2 | C. | NaOH与CO2 | D. | NaAlO2与HNO3 |
分析 A.过氧化钠与二氧化碳反应生成碳酸钠和水、氧气,反应与反应物的用量无关;
B.钠在氧气中放置生成氧化钠,在氧气中点燃生成过氧化钠;
C.氢氧化钠和二氧化碳1:1反应生成碳酸氢钠,按照2:1反应生成碳酸钠;
D.偏铝酸钠和硝酸反应硝酸和偏铝酸钠1:1混合生成氢氧化铝沉淀,硝酸过量生成硝酸铝溶液.
解答 解:A.过氧化钠与二氧化碳反应生成碳酸钠和水、氧气,反应与反应物的用量无关,故A正确;
B.钠在氧气中放置生成氧化钠,在氧气中点燃生成过氧化钠,反应条件不同产物不同,故B错误;
C.氢氧化钠和二氧化碳1:1反应生成碳酸氢钠,按照2:1反应生成碳酸钠,反应物用量不同,产物不同,故C错误;
D.硝酸和偏铝酸钠按照1:1反应生成氢氧化铝沉淀,当硝酸过量生成的氢氧化铝会溶解生成硝酸铝,反应物用量不同,产物不同,故D错误;
故选A.
点评 本题考查了反应条件或反应物的用量对反应的影响,题目难度不大,熟悉物质的性质是解题的关键.

练习册系列答案
相关题目
14.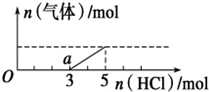 将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发),下列说法不正确的是( )
将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发),下列说法不正确的是( )
 将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发),下列说法不正确的是( )
将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发),下列说法不正确的是( )| A. | O点溶液中所含溶质的化学式为NaOH、Na2CO3 | |
| B. | a点溶液中c (HCO3-)>c (CO32-) | |
| C. | 标准状况下,通入CO2的体积为44.8L | |
| D. | 原NaOH溶液的物质的量浓度为5mol/L |
11.下列离子方程式正确的是( )
| A. | 稀硝酸与氢氧化钠溶液反应:H++OH-=H2O | |
| B. | 铝与稀盐酸反应:Al+2H+=Al3++H2↑ | |
| C. | 三氯化铁溶液与氢氧化钠溶液反应:FeCl3+3OH-=Fe(OH)3↓+3C1- | |
| D. | 二氧化碳与澄清石灰水反应:CO2+2OH-=CO32-+H2O |
18.下列物质能发生消去反应的是( )
| A. | CH3Cl | B. | (CH3)3CCH2Cl | C. | 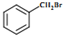 | D. | 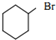 |
8.下列分子为直线形分子且分子中所有原子都满足最外层8电子稳定结构的是( )
| A. | BeCl2 | B. | C2H2 | C. | CO2 | D. | NH3 |
15.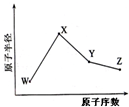 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图.已知W的一种核素的质量数为18,中子数为10,X原子和Ne原子的核外电子数相差1,Y的单质是一种常见的半导体材料,Z的非金属性在同周期元素中最强.下列说法错误的是( )
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图.已知W的一种核素的质量数为18,中子数为10,X原子和Ne原子的核外电子数相差1,Y的单质是一种常见的半导体材料,Z的非金属性在同周期元素中最强.下列说法错误的是( )
 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图.已知W的一种核素的质量数为18,中子数为10,X原子和Ne原子的核外电子数相差1,Y的单质是一种常见的半导体材料,Z的非金属性在同周期元素中最强.下列说法错误的是( )
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图.已知W的一种核素的质量数为18,中子数为10,X原子和Ne原子的核外电子数相差1,Y的单质是一种常见的半导体材料,Z的非金属性在同周期元素中最强.下列说法错误的是( )| A. | 对应简单离子半径X<W | |
| B. | 对应气态氢化物的稳定性Y<Z | |
| C. | 化合物XZW既含离子键又含共价键 | |
| D. | Z或X的最高价氧化物对应的水化物均能与Y的氧化物反应 |
3.某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
(1)催化剂能加快化学反应速率的原因是降低了活化能.
(2)常温下5% H2O2溶液的pH约为6,H2O2的电离方程式为⇒H2O2?H++HO2-.
(3)实验①和②的目的是探究浓度对反应速率的影响.
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图.
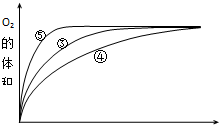
分析上图能够得出的实验结论是碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率.
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol•L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol•L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol•L-1FeCl3溶液 |
(2)常温下5% H2O2溶液的pH约为6,H2O2的电离方程式为⇒H2O2?H++HO2-.
(3)实验①和②的目的是探究浓度对反应速率的影响.
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图.

分析上图能够得出的实验结论是碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率.
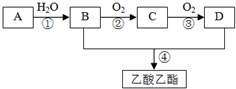 A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平.现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平.现以A为主要原料合成乙酸乙酯,其合成路线如图所示. CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;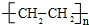 .
.