题目内容
18.改变下列条件,化学平衡一定向正反应方向移动的是( )| A. | 增大反应物浓度 | B. | 升高温度 | C. | 增大压强 |
分析 根据影响平衡移动的因素,增大反应物浓度平衡向正反应方向移动,升高温度平衡向吸热方向移动,增大压强,平衡向气体体积减小的方向移动,据此判断;
解答 解:A、增大反应物浓度平衡向正反应方向移动,故A正确;
B、升高温度平衡向吸热方向移动,对于正反应是吸热的反应平衡向逆反应方向移动,故B错误;
C、增大压强,平衡向气体体积减小的方向移动,对于正反应是气体体积增大的反应,平衡向逆反应方向移动,故C错误;
故选A.
点评 本题考查了化学平衡影响因素的分析判断,平衡移动原理和转化率的变化是解题关键,题目难度不大.

练习册系列答案
相关题目
10.下列电离方程式正确的是( )
| A. | NaHSO4?Na++H++SO42- | B. | HCO3-+H2O═H3O++CO32- | ||
| C. | HClO═H++ClO- | D. | H2S?H++HS- |
11.①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池,①②相连时,外电路电流从①流向②;①③相连时,③为正极;②④相连时,④上有气泡逸出;③④相连时,③的质量减少.据此判断这四种金属活动性由大到小的顺序是( )
| A. | ①③②④ | B. | ①③④② | C. | ②①③④ | D. | ③①②④ |
3.下列反应的离子方程式书写正确的是( )
| A. | 硫酸铝溶液中加入过量氨水 Al3++3OH-═Al(OH)3↓ | |
| B. | 硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液 Fe2++2H++H2O2═Fe3++2H2O | |
| C. | 碳酸钙与醋酸反应 CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | 电解饱和食盐水 2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+C12↑+2OH- |
6.常见的无机酸25℃时在水溶液中的电离平衡常数如下表,下列选项正确的是( )
| 氢氰酸(HCN) | 碳酸(H2CO3) | 氢氟酸(HF) |
| K=6.2×10-10 | Ka1=4.2×10-7 | K=6.61×10-4 |
| A. | 氟化钠溶液中通入CO2:2F-+H2O+CO2═2HF+CO32- | |
| B. | NaCN与HCN的混合溶液中:2c(Na+)═c(CN-)+c(HCN) | |
| C. | 0.2 mol•L-1 HCN溶液与0.1mol•L-1NaOH溶液等体积混合后,溶液的pH>7 | |
| D. | 25℃时同浓度的NaCN和NaF溶液的pH值前者小于后者 |
7.下列各组中的两物质作用时,反应条件或反应物用量的改变,对生成物没有影响的是( )
| A. | N2和H2 | B. | Na和O2 | C. | NaOH和CO2 | D. | C和O2 |
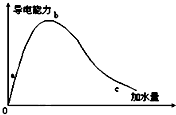 在一定温度下,冰醋酸加水稀释的过程中,溶液的导电能力如图所示,请回答:
在一定温度下,冰醋酸加水稀释的过程中,溶液的导电能力如图所示,请回答:
 2Z 0.1mol·min—1
2Z 0.1mol·min—1