题目内容
 25℃时,在20ml 0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1醋酸溶液,曲线如图所示,有关粒子浓度关系的比较中,不正确的是( )
25℃时,在20ml 0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1醋酸溶液,曲线如图所示,有关粒子浓度关系的比较中,不正确的是( )| A、在A点:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| B、在B点:c(Na+)=c(CH3COO-),c(OH-)=c(H+) |
| C、在C点:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
| D、在C点:c(Na+)=c(CH3COO-)+c(CH3COOH) |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:这是一道以中和滴定为背景,以图象呈现为方式的离子浓度大小比较题.
在A点时消耗0.2mol/L醋酸溶液10mL,两者恰好完全反应生成CH3COONa,溶液呈碱性;
在B点时溶液呈中性,即c(OH-)=c(H+),则c(Na+)=c(CH3COO-),此时必须醋酸稍过量;
在C点时所加入醋酸的物质的量是NaOH的物质的量的2倍.醋酸过量,所得溶液中C(CH3COOH)=C(CH3COONa),溶液呈酸性.据此分析.
在A点时消耗0.2mol/L醋酸溶液10mL,两者恰好完全反应生成CH3COONa,溶液呈碱性;
在B点时溶液呈中性,即c(OH-)=c(H+),则c(Na+)=c(CH3COO-),此时必须醋酸稍过量;
在C点时所加入醋酸的物质的量是NaOH的物质的量的2倍.醋酸过量,所得溶液中C(CH3COOH)=C(CH3COONa),溶液呈酸性.据此分析.
解答:
解:A.在A点醋酸和NaOH恰好中和生成NaAc,为强碱弱酸盐,水解呈碱性,但Ac-水解程度较小,应为c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故A正确;
B、B点呈中性,应为C(Na+)=C(Ac-)>C(OH-)=C(H+),故B正确;
C、在C点的溶液中有Na+、Ac-、OH-、H+,根据电荷守恒可有:c(Na+)+c(H+)=c(CH3COO-)+c(OH-),故C正确;
D、C点时,n(NaOH)=0.02L×0.1mol/L=0.002mol,n(HAc)=0.02mol/L×0.02L=0.004mol,根据物料守恒可知c(Ac-)+c(HAc)=2c(Na+),故D错误;
故选D.
B、B点呈中性,应为C(Na+)=C(Ac-)>C(OH-)=C(H+),故B正确;
C、在C点的溶液中有Na+、Ac-、OH-、H+,根据电荷守恒可有:c(Na+)+c(H+)=c(CH3COO-)+c(OH-),故C正确;
D、C点时,n(NaOH)=0.02L×0.1mol/L=0.002mol,n(HAc)=0.02mol/L×0.02L=0.004mol,根据物料守恒可知c(Ac-)+c(HAc)=2c(Na+),故D错误;
故选D.
点评:本题考查酸碱混合溶液PH的判断与计算,题目难度较大,注意从电解质的强弱以及酸碱混合反应的角度分析,注意分析曲线的变化特点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
有关玻璃棒在实验中的用途及操作中,不正确的是( )
①物质溶解时用玻璃棒搅拌;
②用玻璃棒蘸少量溶液做焰色反应;
③测溶液pH时用玻璃棒蘸溶液;
④过滤时引流,玻璃棒下端靠在漏斗内滤纸的任意部位;
⑤配制一定物质的量浓度的溶液时要用玻璃棒引流;
⑥加热坩埚中硫酸铜晶体时用玻璃棒搅拌.
①物质溶解时用玻璃棒搅拌;
②用玻璃棒蘸少量溶液做焰色反应;
③测溶液pH时用玻璃棒蘸溶液;
④过滤时引流,玻璃棒下端靠在漏斗内滤纸的任意部位;
⑤配制一定物质的量浓度的溶液时要用玻璃棒引流;
⑥加热坩埚中硫酸铜晶体时用玻璃棒搅拌.
| A、①⑤ | B、③⑥ | C、②⑥ | D、②④ |
已知(CH3)2C=CH2可表示为 ,脱落酸属植物生长抑制剂,对该物质叙述正确的( )
,脱落酸属植物生长抑制剂,对该物质叙述正确的( )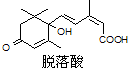
 ,脱落酸属植物生长抑制剂,对该物质叙述正确的( )
,脱落酸属植物生长抑制剂,对该物质叙述正确的( )
| A、分子式为C15H22O4 |
| B、分子中所有碳原子可以在同一平面上 |
| C、1mol该物质最多可与3mol H2发生反应 |
| D、在一定条件下发生反应生成含七元环的物质 |
尼泊金酯是对羟基苯甲酸  与醇形成的酯类化合物,主要用作有机合成、食品、化妆品、医药的杀菌防腐剂,也用作于饲料防腐剂.下列说法中正确的是( )
与醇形成的酯类化合物,主要用作有机合成、食品、化妆品、医药的杀菌防腐剂,也用作于饲料防腐剂.下列说法中正确的是( )
 与醇形成的酯类化合物,主要用作有机合成、食品、化妆品、医药的杀菌防腐剂,也用作于饲料防腐剂.下列说法中正确的是( )
与醇形成的酯类化合物,主要用作有机合成、食品、化妆品、医药的杀菌防腐剂,也用作于饲料防腐剂.下列说法中正确的是( )| A、尼泊金乙酯与NaOH溶液反应时,可消耗1mol NaOH |
| B、尼泊金乙酯分子结构中,至少有6个碳原子在一个平面内 |
| C、尼泊金丁酯最多可与4mol H2发生加成反应 |
D、尼泊金丁酯是由对羟基苯甲酸与1-丁醇形成的酯,结构简式如图: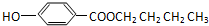 |
关于图,下列说法不正确的是( )
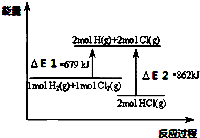

| A、△E1是该反应的活化能 |
| B、△E2是破坏2mol HCl(g)所需的能量 |
| C、该反应的热化学方程式为:H2+Cl2=2 HCl△H=-183KJ/mol |
| D、该反应是一个反应物总能量高于生成物总能量的反应 |
通过对实验现象的观察、分析推理得出正确的结论,这是化学学习的方法之一.对下列实验事实解释正确的是( )
| A、浓HNO3在光照条件下变黄浓硝酸不稳定,生成的有色产物能溶于浓硝酸 |
| B、K I淀粉溶液中通入适量Cl2,溶液变蓝Cl2能与淀粉发生显色反应 |
| C、向某溶液中加硝酸酸化的氯化钡溶液,有白色沉淀生成说明该溶液中含有SO42- |
| D、向盐酸中加入浓硫酸时产生白雾说明浓硫酸具有脱水性 |
