题目内容
1.2molCl2与元素A单质完全反应生成0.80molAClx,则x值为 .
考点:化学方程式的有关计算
专题:计算题
分析:氯气完全反应生成AClx,根据氯原子守恒列方程计算x的值.
解答:
解:1.2molCl2与足量的元素A的单质完全反应生成0.80mol AClx,
根据Cl原子守恒有:1.2mol×2=0.8mol×x,解得x=3,
故答案为:3.
根据Cl原子守恒有:1.2mol×2=0.8mol×x,解得x=3,
故答案为:3.
点评:本题考查化学方程式的计算,注意根据原子守恒计算,比较基础.

练习册系列答案
相关题目
给物质分类时由于标准不同往往会出现( )
| A、树状分类法 |
| B、环状分类法 |
| C、球状分类法 |
| D、交叉分类法 |
叠氮酸钠(NaN3)是抗禽流感药物“达菲”合成过程中的中间活性物质,3molNaN3受撞击会生成4mol氮气和一种离子化合物(Na3N).下列有关叙述错误的是( )
| A、NaN3受撞击时,NaN3既是氧化剂又是还原剂 |
| B、Na3N中Na+半径比N3-半径小 |
| C、NaN3跟水反应时,有NH3生成 |
| D、NaN3中,既存在离子键又存在非极性共价键 |
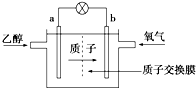 美国圣路易斯大学科学家研制了一种新型的乙醇电池(DEFC),它用磺酸类质子(H+)作溶剂,在200℃左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全.电池总反应式为C2H5OH+3O2═2CO2+3H2O,电池示意图如图所示.下列说法不正确的是( )
美国圣路易斯大学科学家研制了一种新型的乙醇电池(DEFC),它用磺酸类质子(H+)作溶剂,在200℃左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全.电池总反应式为C2H5OH+3O2═2CO2+3H2O,电池示意图如图所示.下列说法不正确的是( )| A、a为电池的负极 |
| B、b电极发生氧化反应 |
| C、电池工作时电流由a极沿导线经灯泡再到b极 |
| D、电池正极的电极反应为:4H++O2+4e-═2H2O |