题目内容
10.某温度下,CuSO4饱和溶液的质量分数为a%,取一定量的此饱和溶液,向其中加入m g无水CuSO4,在温度不变的情况下析出W g CuSO4•5H2O晶体,则原饱和溶液中溶质CuSO4的质量减少( )| A. | m×a% | B. | W×a% | C. | (m+W)×a% | D. | (W-m)×a% |
分析 根据溶液析出水合物后仍是饱和溶液,W克水合物中,分为两部分,一部分是加入的m克的无水盐;另一部分是饱和溶液的一部分,从原溶液中析出的溶质就在这部分里,而饱和溶液的溶质质量分数已知,则饱和溶液减少的质量为(W-m)g.然后利用饱和溶液中,溶质的质量=溶液的质量×饱和溶液的质量分数进行计算.
解答 解:由题意可知,原溶液为饱和溶液,则加入mg该无水盐后晶体析出后的溶液仍然为饱和溶液,则饱和溶液减少的质量为(W-m)g也是饱和溶液,由一定温度下,某无水盐在水中溶质的质量分数为a%,从原饱和溶液中析出溶质的质量为x,则$\frac{x}{W-m}$×100%=a%,x=(W-m)×a%,
故选D.
点评 本题考查学生饱和溶液中溶质质量的计算方法,依据饱和溶液中溶质的质量分数计算即可,关键是分析饱和溶液中的溶质和溶液的质量.

练习册系列答案
相关题目
20.肼(N2H4)能与硫酸反应生成N2H6SO4,已知N2H6SO4的晶体类型与硫酸铵相同,则N2H6SO4晶体内不存在( )
| A. | 离子键 | B. | 共价键 | C. | 配位键 | D. | 范德华力 |
18.如图,将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中,下列分析正确的是( )
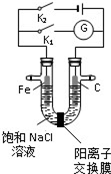

| A. | K1闭合,铁棒侧溶液会出现白色沉淀,而且沉淀最终变为红褐色 | |
| B. | K1或 K2闭合,石墨棒周围溶液 pH 均升高 | |
| C. | K2闭合,铁棒上发生的反应为 2Cl--2e-═Cl2↑ | |
| D. | K2闭合,电路中通过 0.002NA个电子时,两极共产生 0.002mol 气体 |
5.传统饮用水的消毒剂是氯气.二十世纪八十年代初期科研人员在英国某城调查发现,儿童患白血病发病率高是源于饮用了氯气消毒的饮用水,这是因为( )
| A. | 氯气有氧化性,作用于正常细胞而癌化 | |
| B. | 氯水中的次氯酸具有杀菌性,氧化了正常细胞,异化为癌细胞 | |
| C. | 氯气有毒,杀死正常细胞,不杀灭癌细胞 | |
| D. | 氯气作用于水中有机物,生成有机氯化合物而致癌 |
15.下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A. | 1 mol聚乙烯含有的原子数目为6NA | |
| B. | 标准状况下1 L己烷完全燃烧后恢复至原状态,生成气态物质分子数为$\frac{5{N}_{A}}{22.4}$ | |
| C. | 1 mol甲基含10NA个电子 | |
| D. | 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
2.下列五种物质中均含有氮元素,它们按下列顺序排列:
①NH3②N2③NO④X⑤HNO3根据这种排列规律,X可能是( )
①NH3②N2③NO④X⑤HNO3根据这种排列规律,X可能是( )
| A. | N2O | B. | NO2 | C. | N2O5 | D. | NaNO2 |
19.铝合金在日常生活、航空航天和汽车制造等方面均有广泛用途.下列关于铝的说法正确的是( )
| A. | 铝的表面容易形成致密的氧化膜,抗腐蚀性能好 | |
| B. | 常温下不与任何酸、碱反应 | |
| C. | 铝元素在地壳中的含量高,储量丰富,仅次于铁 | |
| D. | 工业上通常用钠与铝盐溶液反应来制备铝 |
20.在由氧化铜和氧化铁组成的a g混合物中,取其一半加入2mol•L-1的稀盐酸溶液50mL,固体恰好完全溶解;若将原混合物在过量的CO气流中加热充分反应,冷却后剩余固体的质量为( )
| A. | 1.6a g | B. | (a-1.6)g | C. | (a-3.2)g | D. | (2a-3.2)g |