题目内容
综合应用题:
Ⅰ.有下列物质:①Fe ②CO2③Na2O ④Cu(OH)2⑤MgCl2⑥NH4Cl ⑦H2SO4⑧C2H5OH(酒精)(用序号作答).其中属于电解质的有 ,属于非电解质的有 .
Ⅱ.今有K2SO4和Al2(SO4)3的混合溶液,已知其中K+浓度是0.2mol?L-1,SO42-的浓度是0.7mol?L-1.
(1)写出Al2(SO4)3电离的电离方程式: .
(2)Al3+浓度应等于 mol?L-1.
Ⅲ.根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
(1)该反应中氧化剂是 ,氧化产物是 .
(2)该反应中被氧化的物质与被还原的物质物质的量之比为 .
(3)用单线桥法标出电子转移的方向与数目 .
Ⅰ.有下列物质:①Fe ②CO2③Na2O ④Cu(OH)2⑤MgCl2⑥NH4Cl ⑦H2SO4⑧C2H5OH(酒精)(用序号作答).其中属于电解质的有
Ⅱ.今有K2SO4和Al2(SO4)3的混合溶液,已知其中K+浓度是0.2mol?L-1,SO42-的浓度是0.7mol?L-1.
(1)写出Al2(SO4)3电离的电离方程式:
(2)Al3+浓度应等于
Ⅲ.根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
(1)该反应中氧化剂是
(2)该反应中被氧化的物质与被还原的物质物质的量之比为
(3)用单线桥法标出电子转移的方向与数目
考点:电解质与非电解质,电离方程式的书写,氧化还原反应
专题:氧化还原反应专题,电离平衡与溶液的pH专题
分析:Ⅰ.电解质:在水溶液中或熔融状态下能够导电的化合物;非电解质:在熔融状态和水溶液中都不能导电的化合物;
II.(1)硫酸铝是强电解质完全电离生成硫酸根离子和铝离子;(2)溶液呈中性,根据电荷守恒求解;
Ⅲ.(1)8NH3+3Cl2=6NH4Cl+N2,氮元素化合价升高,发生氧化反应,氯元素化合价降低发生还原反应,据此解答;
(2)该反应中,氯气中的氯元素化合价全部降低,氨气中的氮元素只有
化合价升高,据此解答;
(3)反应中N元素的化合价由-3升高为0,Cl元素的化合价0降低为-1价,氨气作还原剂,氯气作氧化剂,该反应生成1mol氮气转移6mol电子.
II.(1)硫酸铝是强电解质完全电离生成硫酸根离子和铝离子;(2)溶液呈中性,根据电荷守恒求解;
Ⅲ.(1)8NH3+3Cl2=6NH4Cl+N2,氮元素化合价升高,发生氧化反应,氯元素化合价降低发生还原反应,据此解答;
(2)该反应中,氯气中的氯元素化合价全部降低,氨气中的氮元素只有
| 1 |
| 4 |
(3)反应中N元素的化合价由-3升高为0,Cl元素的化合价0降低为-1价,氨气作还原剂,氯气作氧化剂,该反应生成1mol氮气转移6mol电子.
解答:
解:Ⅰ.①Fe为金属单质,既不是电解质也不是非电解质;
②CO2自身不能电离,是非电解质;
③Na2O在熔融状态下能够导电,是电解质;
④Cu(OH)2在水溶液中能够导电,是电解质;
⑤MgCl2在水溶液中或熔融状态下能够导电,是电解质;
⑥NH4Cl在水溶液中能够导电,是电解质;
⑦H2SO4在水溶液中能够导电,是电解质;
⑧C2H5OH(酒精)在熔融状态和水溶液中都不能导电,是非电解质;
故属于电解质的是③④⑤⑥⑦;属于非电解质的是②⑧,
故答案为:③④⑤⑥⑦;②⑧;
II.(1)硫酸铝是强电解质完全电离,电离方程式:Al2(SO4)3=2Al3++3SO42-;
故答案为:Al2(SO4)3=2Al3++3SO42-;
(2)溶液呈中性,根据电荷守恒列关系式:C(Al3+)×3+C(K+)=2×C(SO42-),将各种离子浓度带入得:C(Al3+)×3+0.2mol?L-1=2×0.7mol?L-1.
C(Al3+)=0.4mol/L;
故答案为:0.4;
Ⅲ.(1)该反应氨气中的氯气中的氯元素化合价降低,所以氯气是氧化剂;氮元素化合价升高,被氧化成氮气;
故答案为:Cl2或氯气;N2或氮气;
(2)在反应8NH3+3Cl2=6NH4Cl+N2,3mol氯气中的氯元素化合价都降低,所以3mol氯气都做氧化剂被还原;8mol氨气中只有2mol氨气中的氮元素化合价升高被氧化,所以做还原剂的氨气只有2mol,该反应中被氧化的物质与被还原的物质物质的量之比为2:3;
故答案为:2:3;
(3)反应中N元素的化合价由-3升高为0,Cl元素的化合价0降低为-1价,2molNH3作还原剂转移电子为6mol,则反应电子转移的方向和数目为 ,
,
故答案为: .
.
②CO2自身不能电离,是非电解质;
③Na2O在熔融状态下能够导电,是电解质;
④Cu(OH)2在水溶液中能够导电,是电解质;
⑤MgCl2在水溶液中或熔融状态下能够导电,是电解质;
⑥NH4Cl在水溶液中能够导电,是电解质;
⑦H2SO4在水溶液中能够导电,是电解质;
⑧C2H5OH(酒精)在熔融状态和水溶液中都不能导电,是非电解质;
故属于电解质的是③④⑤⑥⑦;属于非电解质的是②⑧,
故答案为:③④⑤⑥⑦;②⑧;
II.(1)硫酸铝是强电解质完全电离,电离方程式:Al2(SO4)3=2Al3++3SO42-;
故答案为:Al2(SO4)3=2Al3++3SO42-;
(2)溶液呈中性,根据电荷守恒列关系式:C(Al3+)×3+C(K+)=2×C(SO42-),将各种离子浓度带入得:C(Al3+)×3+0.2mol?L-1=2×0.7mol?L-1.
C(Al3+)=0.4mol/L;
故答案为:0.4;
Ⅲ.(1)该反应氨气中的氯气中的氯元素化合价降低,所以氯气是氧化剂;氮元素化合价升高,被氧化成氮气;
故答案为:Cl2或氯气;N2或氮气;
(2)在反应8NH3+3Cl2=6NH4Cl+N2,3mol氯气中的氯元素化合价都降低,所以3mol氯气都做氧化剂被还原;8mol氨气中只有2mol氨气中的氮元素化合价升高被氧化,所以做还原剂的氨气只有2mol,该反应中被氧化的物质与被还原的物质物质的量之比为2:3;
故答案为:2:3;
(3)反应中N元素的化合价由-3升高为0,Cl元素的化合价0降低为-1价,2molNH3作还原剂转移电子为6mol,则反应电子转移的方向和数目为
 ,
,故答案为:
 .
.
点评:本题考查了电解质和非电解质的判断,物质的量、物质的量浓度的相关计算,氧化还原反应的概念和表示方法,注意Ⅲ中的(2)是易错项.

练习册系列答案
 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
下列关于有机物的命名中不正确的是( )
| A、2,2─二甲基戊烷 |
| B、2─乙基戊烷 |
| C、3,4─二甲基辛烷 |
| D、3─甲基己烷 |
在密闭容器中发生下列反应:aA(g)?cC(g)+dD(g),反应达到平衡后,将容积扩大为原来的2倍,当再次达到平衡时,D的浓度为原来平衡的0.3倍,下列叙述正确的是( )
| A、平衡向正反应方向移动 |
| B、a>c+d |
| C、D的体积分数变大 |
| D、A的转化率变大 |
下列操作,能使水的电离平衡向右移动,且使所得溶液显酸性的是( )
| A、在水中加入少量氯化钠,并加热到100℃ |
| B、在水中滴人稀硫酸 |
| C、在水中加入小苏打 |
| D、在水中加入氯化铝固体 |
下列图示与对应的叙述相符的是( )
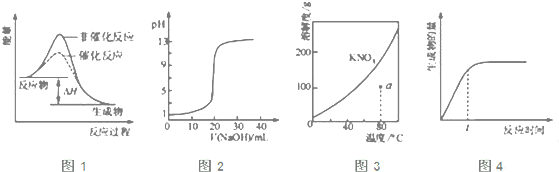

| A、图1表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| B、图2表示0.1000 mol?L-1NaOH溶液滴定20.00mL0.1000 mol?L-1CH3COOH溶液所得到的滴定曲线 |
| C、图3表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 |
| D、图4表示某可逆反应生成物的量随反应时间变化的曲线,由图知t时v正<v逆 |
下列事实不能用勒夏特列原理解释的是( )
| A、由H2、I2(g)、HI组成的平衡体系加压后颜色变深 |
| B、黄绿色的氯水光照后颜色变浅 |
| C、使用催化剂可加快SO2转化为SO3的速率 |
| D、在含有Fe(SCN)2+的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去 |
四种短周期元素的性质或结构信息如下表,下列推断错误的是( )
| 元素编号 | 元素性质或结构 |
| T | M层上有2对成对电子 |
| X | 元素最高正价是+7价 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | 单质是银白色固体、导电、密度比水小,与水剧烈反应、和氧气反应不同条件下产物不同 |
| A、T的氢化物是同周期元素氢化物中最不稳定的 |
| B、X的最高价氧化物对应的水化物,是无机含氧酸中的最强酸 |
| C、离子半径从小到大的顺序:Y<Z<T<X |
| D、X、T形成化合物的类型与X、Z形成化合物的类型不同 |