题目内容
5. 乙酸是食醋的主要成分,它具有以下化学性质:
乙酸是食醋的主要成分,它具有以下化学性质:(1)可使紫色石蕊试液变红色,说明乙酸具有酸性.
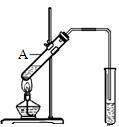
(2)能发生酯化反应.实验室用图所示装置制取乙酸乙酯,在试管A中加入的试剂有浓硫酸、冰醋酸(CH3COOH)和乙醇(填写名称).请写出该反应的化学方程式:CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O.
分析 (1)乙酸含-COOH,具有酸性,能使紫色石蕊变红;
(2)乙醇、乙酸在浓硫酸作用下发生酯化反应生成乙酸乙酯和水,以此来解答.
解答 解:(1)乙酸可使紫色石蕊试液变红色,说明乙酸具有酸性,故答案为:红;酸;
(2)乙酸能发生酯化反应.实验室用图所示装置制取乙酸乙酯,在试管A中加入的试剂有浓硫酸、冰醋酸(CH3COOH)和乙醇,该反应的化学方程式为CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O,
故答案为:乙醇;CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O.
点评 本题考查有机物的结构与性质,为高频考点,把握乙酸、乙醇的性质为解答的关键,侧重分析与应用能力的考查,注意官能团与性质的关系,题目难度不大.

练习册系列答案
相关题目
13.已知反应H2(g)+I2(g)═2HI(g),1mol H2完全反应放出a kJ的热量,依据下表数据,以下说法错误的是
( )
( )
| 化 学 键 | H-H | I-I |
| 断开1mol化学键时吸收的能量(kJ) | b | c |
| A. | 该反应中反应物的总能量高于生成物的总能量 | |
| B. | 断开1 mol H-H 键和1 mol I-I 键所需能量大于断开2 mol H-I 键所需能量 | |
| C. | 断开2 mol H-I键所需能量为(a+b+c)kJ | |
| D. | 向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ |
20. 2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
 2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
2SO2(g)+O2(g)?2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A. | △H=E2-E1 | |
| B. | 反应物断键吸收的总能量小于生成物成键释放的总能量 | |
| C. | 升高温度,不影响活化分子百分数 | |
| D. | 使用催化剂使该反应的反应热发生改变 |
17.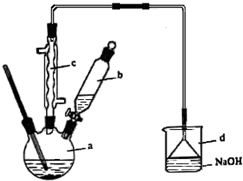 溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴,回答下列问题:
(1)c仪器的名称是球形冷凝管,向a中滴加几滴溴,有白雾产生,是因为生成了HBr气体,a中发生反应的化学方程式为 .该反应的类型是取代反应;装置d的作用是吸收HBr和Br2;
.该反应的类型是取代反应;装置d的作用是吸收HBr和Br2;
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤,NaOH溶液洗涤的作用是除去HBr和未反应的Br2;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤,加入氯化钙的目的是吸水(干燥).
(3)经过上述分离操作后,粗溴苯中还含有的主要杂质为苯,要进一步提纯,应选择下列C操作(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取.
 溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
(1)c仪器的名称是球形冷凝管,向a中滴加几滴溴,有白雾产生,是因为生成了HBr气体,a中发生反应的化学方程式为
 .该反应的类型是取代反应;装置d的作用是吸收HBr和Br2;
.该反应的类型是取代反应;装置d的作用是吸收HBr和Br2;(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤,NaOH溶液洗涤的作用是除去HBr和未反应的Br2;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤,加入氯化钙的目的是吸水(干燥).
(3)经过上述分离操作后,粗溴苯中还含有的主要杂质为苯,要进一步提纯,应选择下列C操作(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取.
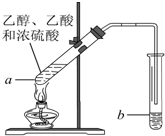 在实验室可以在试管a中加入3mL 乙醇,然后边振荡试管边慢慢加入2mL浓硫酸和2mL 乙酸,按下图所示,连接好装置进行实验,以制取乙酸乙酯.回答下列问题:
在实验室可以在试管a中加入3mL 乙醇,然后边振荡试管边慢慢加入2mL浓硫酸和2mL 乙酸,按下图所示,连接好装置进行实验,以制取乙酸乙酯.回答下列问题: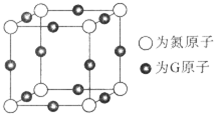 A、B、C、D、E、F、G是前四周期(除稀有气体)原子序数依次增大的七种元素,A的原子核外电子只有一种运动状态;B、C的价电子层中未成对电子数都 是2;B、C、D同周期;E核外的s、p能级的电子总数相;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满.回答下列问题:(相关问题用元素符号表示)
A、B、C、D、E、F、G是前四周期(除稀有气体)原子序数依次增大的七种元素,A的原子核外电子只有一种运动状态;B、C的价电子层中未成对电子数都 是2;B、C、D同周期;E核外的s、p能级的电子总数相;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满.回答下列问题:(相关问题用元素符号表示)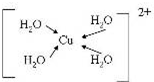 (配位键用→标出).
(配位键用→标出). 为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):