题目内容
9.将一定量的Al、Mg合金加入到足量的40mL某浓度的盐酸中,充分反应后得到标准状况下的氢气896mL;若将等质量的该混合物加入到足量的NaOH溶液中,充分反应后得到标准状况下的氢气672mL.(1)当合金与盐酸反应时,转移电子总物质的量为0.08mol;
(2)合金中Mg的质量为0.24g;
(3)合金的平均摩尔质量为26g/mol;
(4)若向与盐酸反应后的溶液中缓慢加入100mL 1mol/L 的NaOH溶液,沉淀质量恰好达到的最大值,则加入盐酸的浓度为2.5mol/L.
分析 与盐酸反应时发生Mg+2HCl=MgCl2+H2↑、2Al+6HCl═2AlCl3+3H2↑,等质量混合物与NaOH反应时发生2Al+2NaOH+2H2O═2NaAlO2+3H2↑,结合n=$\frac{V}{Vm}$、M=$\frac{m}{n}$、电子守恒、原子守恒计算.
解答 解:(1)与盐酸反应生成的氢气为$\frac{0.896L}{22.4L/mol}$=0.04mol,由H元素的化合价变化可知,转移电子=得到电子=0.04mol×2×(1-0)=0.08mol,
故答案为:0.08;
(2)与NaOH反应生成的氢气为$\frac{0.672L}{22.4L/mol}$=0.03mol,可知等质量混合物中含Al为0.02mol,Mg与盐酸反应生成的氢气为0.04mol-0.03mol=0.01mol,由Mg+2HCl=MgCl2+H2↑可知,n(Mg)=0.01mol,其质量为0.01mol×24g/mol=0.24g,
故答案为:0.24;
(3)合金的平均摩尔质量为$\frac{0.01mol×24g/mol+0.02mol×27g/mol}{0.03mol}$=26g/mol,
故答案为:26g/mol;
(4)若向与盐酸反应后的溶液中缓慢加入100mL 1mol/L 的NaOH溶液,沉淀质量恰好达到的最大值,溶质为NaCl,由原子守恒可知,n(HCl)=n(NaCl)=n(NaOH)=0.1L×1mol/L=0.1mol,加入盐酸的浓度为$\frac{0.1mol}{0.04L}$=2.5mol/L,
故答案为:2.5.
点评 本题考查氧化还原反应的计算,为高频考点,把握发生的反应、电子守恒及原子守恒为解答的关键,侧重分析与计算能力的考查,注意混合物中Al与NaOH反应,题目难度不大.

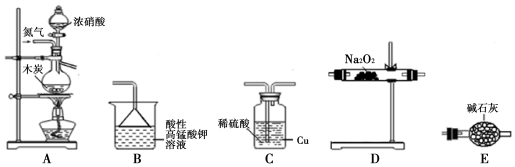
已知:①2NO+Na2O2═2NaNO2;
②酸性条件下,NO、NO2都能与MnO4-反应生成NO3-和Mn2+;NaNO2能使
酸性高锰酸钾溶液褪色.
(1)实验装置的连接顺序为ACEDEB;
(2)C瓶内发生反应的离子方程式为Cu+2H++NO2=Cu2++NO+H2O.
(3)为了测定亚硝酸钠的含量,称取4.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.10mol•L-1的酸性KMnO4溶液进行滴定,实验所得数据如表.
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶用蒸馏水洗净后未干燥
c.观察滴定终点时仰视读数
②根据表中数据进行计算,所制得的固体中亚硝酸钠的质量分数为86.25%.
(4)设计实验,比较0.1mol•L-1NaNO2溶液中NO2-的水解程度和0.1mol•L-1HNO2溶液中HNO2电离程度的相对大小25℃时,将两种溶液等体积混合,若混合溶液的pH<7,则说明HNO2的电离程度大于NO2-的水解程度;若pH>7,则说明HNO2的电离程度小于NO2-的水解程度(简要说明实验步骤、现象和结论,仪器和药品自选).
| 实验操作 | 实验目的或结论 | |
| A | 蘸有浓硝酸的玻璃棒靠近浓氨水时冒白烟 | NH3具有还原性 |
| B | 将一块Na放入乙醇溶液中,有气泡产生 | Na能置换乙醇中的氢 |
| C | 可将58.5gNaCl加入盛有500mL水的烧杯中,搅拌、溶解 | 粗略配置浓度为2mol•L-1的NaCl溶液 |
| D | 向氯仿中加入NaOH溶液,加热充分反应后,再加入AgNO3 | 验证氯仿中含有的氯元素 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 2.3g钠由原子变成离子时,失去的电子数为0.2 NA | |
| B. | 0.2 NA个硫酸分子与19.6g磷酸(H3PO4)含有相同的氧原子数 | |
| C. | 28g氮气所含的原子数为NA | |
| D. | NA个氧分子与NA个氢分子的质量比为8:1 |
| A. | (Υ1+Υ2-Υ3)L | B. | (Υ1+Υ2+Υ3)L | C. | (Υ1+Υ2-2Υ3)L | D. | [Υ3-(Υ1+Υ2)]L |
| A. | O、Na、S | B. | I、Br、Cl | C. | Al、Si、P | D. | Li、Na、K |
| A. |  量筒 | B. |  蒸发皿 | C. | 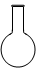 烧瓶 | D. |  分液漏斗 |
①稳定性:HCl>H2S>PH3
②离子半径:O2->F->Na+>Mg2+>Al3+
③碱性:NaOH>KOH>Ca(OH)2>Mg(OH)2
④最高化合价:Cl>Si>Al>F
⑤沸点:HF>HCl>HBr>HI.
| A. | ①②④⑤ | B. | ①②④ | C. | ①②⑤ | D. | ①④⑤ |
| A. | 酒精可用来消毒是由于其具有强氧化性 | |
| B. | 电能、地热能、生物质能均为一次能源 | |
| C. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 | |
| D. | 明矾可用于净水,是因为生成的胶体具有吸附作用 |