题目内容
在原子序数为1-18号元素中,与水反应最剧烈的金属元素是 ; 化学方程式为 .与H2反应最剧烈的非金属元素是 ;化学方程式为 .其中第三周期中,原子半径最大的金属元素是 ; 元素的最高价氧化物所对应的酸最强的是 .并用电子式表示MgBr2的形成过程 .
考点:元素周期律的作用
专题:元素周期律与元素周期表专题
分析:元素周期表中的递变规律:同周期元素的原子,从左到右,原子半径逐渐减小,元素的金属性逐渐减弱,非金属性逐渐增强;和氢气反应越来越剧烈,生成的氢化物稳定性逐渐增强;最高价氧化物对应水化物的酸性逐渐增强;从下到上,原子半径逐渐减小,元素的金属性逐渐减弱,非金属性逐渐增强;氢气反应越来越剧烈,生成的氢化物稳定性逐渐增强;原子半径逐渐减小;最高价氧化物对应水化物的酸性逐渐增强,据此来回答.
解答:
解:根据元素周期律:同周期元素的原子,从左到右,元素的金属性逐渐减弱,从下到上,元素的金属性逐渐减弱,所以与水反应最剧烈的金属元素是Na,反应为:2Na+2H2O=2NaOH+H2↑,同周期元素的原子,从左到右,和氢气反应越来越剧烈,同主族元素的原子,从下到上,和氢气反应越来越剧烈,与H2反应最剧烈的非金属元素是F,即F2+H2=2HF,同周期元素的原子,从左到右,原子半径逐渐减小,最高价氧化物对应水化物的酸性逐渐增强,第三周期中,原子半径最大的金属元素是Na,元素的最高价氧化物所对应的酸最强的是HClO4,MgBr2的形成过程为: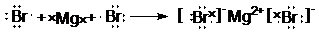 .
.
故答案为:Na;2Na+2H2O=2NaOH+H2↑;F;F2+H2=2HF;Na;HClO4; .
.
 .
.故答案为:Na;2Na+2H2O=2NaOH+H2↑;F;F2+H2=2HF;Na;HClO4;
 .
.
点评:本题考查学生元素周期表中的递变规律,注意知识的归纳和整理是解题的关键,难度不大.

练习册系列答案
相关题目
已知3.6g碳在6.4g的氧气中燃烧,至反应物耗尽,放出X kJ热量.已知单质碳的热值为-
kJ?g-1,则C与1mol O2反应生成CO时的反应热△H为( )
| Y |
| 12 |
| A、-Y kJ?mol-1 |
| B、-(10X-Y) kJ?mol-1 |
| C、-(5X-0.5Y) kJ?mol-1 |
| D、+(10X-Y) kJ?mol-1 |
 某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度.
某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度.