��Ŀ����
16�������£�H2SO3�ĵ��볣��Ka1=1.2��10-2��Ka2=6.3��10-8��H2CO3�ĵ��볣��Ka1=4.5��10-7��Ka2=4.7��10-11��ijͬѧ���ʵ����֤H2SO3����ǿ��H2CO3����SO2��CO2����ֱ�ͨ��ˮ�������ͣ�������pH�Ʋ�����Һ��pH����ǰ�ߵ�pHС�ں��ߣ���H2SO3����ǿ��H2CO3����1����ʵ����Ʋ���ȷ�������������ڱȽ�pH������������ʵ���Ũ�Ȳ���ȣ�
��2����ƺ���ʵ����֤H2SO3����ǿ��H2CO3���ɹ�ѡ����Լ���1mol•L-1Na2CO3��1mol•L-1NaHCO3��1mol•L-1Na2SO3��1mol•L-1NaHSO3��pH�ƣ�
��Ҫ˵��ʵ�鲽�衢����ͽ���������ͬ���ʵ���Ũ�ȵ�NaHSO3��NaHCO3��Һ������ȼƣ���pH��ֽ��������Һ��pH��ǰ�ߵ�pHС�ں��ߣ�֤��H2SO3����ǿ��H2CO3��
��3�������������ݣ�д��������SO2����ͨ��Na2CO3��Һ�еĻ�ѧ����ʽSO2+H2O+2Na2CO3=2NaHCO3+Na2SO3��
��4��Na2CO3��Һ�׳ƴ�������ӷ���ʽ��ʾ��ԭ��CO32-+H2O?HCO3-+OH-��������÷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ2.13��10-4��
���� ��1��H2SO3��H2CO3�����ڶ�Ԫ�ᣬҪ��ͨ���Ƚ϶��ߵ�pH����֤���ߵ�����ǿ��������ʹ���ߵ�Ũ����ͬ������SO2��CO2��������ˮ��ı�����Һ��Ũ����Ȼ����ȣ���Ϊ���ߵ��ܽ�Ȳ�ͬ�������Ը�ʵ����Ʋ���ȷ��
��2��Ҫ��������ǿ�������Բ��ö��ַ�������������ˮ��ԭ������Խ����Ӧ��ǿ���ξ�Խ��ˮ�⣩��Ҳ�������ý�ǿ������ȡ�������������飻
��3��������SO2����ͨ��Na2CO3��Һ�з�Ӧ����̼�����ƺ��������ƣ�
��4��Na2CO3��ǿ�������Σ�CO32-ˮ�����Һ�ʼ��ԣ�ƽ�ⳣ��K=$\frac{c��O{H}^{-}��c��HC{{O}_{3}}^{-}��}{c��C{{O}_{3}}^{2-}��}$��
��� �⣺��1��H2SO3��H2CO3�����ڶ�Ԫ�ᣬҪ��ͨ���Ƚ϶��ߵ�pH����֤���ߵ�����ǿ��������ʹ���ߵ�Ũ����ͬ������SO2��CO2��������ˮ��ı�����Һ��Ũ����Ȼ����ȣ���Ϊ���ߵ��ܽ�Ȳ�ͬ�������Ը�ʵ����Ʋ���ȷ��
��2��Ҫ��������ǿ�������Բ��ö��ַ�������������ˮ��ԭ������Խ����Ӧ��ǿ���ξ�Խ��ˮ�⣩��Ҳ�������ý�ǿ������ȡ��������������ʴ�Ϊ�����ڱȽ�pH������������ʵ���Ũ�Ȳ���ȣ�������ͬ���ʵ���Ũ�ȵ�NaHSO3��NaHCO3��Һ������ȼƣ���pH��ֽ��������Һ��pH��ǰ�ߵ�pHС�ں��ߣ�֤��H2SO3����ǿ��H2CO3��
�ʴ�Ϊ��������ͬ���ʵ���Ũ�ȵ�NaHSO3��NaHCO3��Һ������ȼƣ���pH��ֽ��������Һ��pH��ǰ�ߵ�pHС�ں��ߣ�֤��H2SO3����ǿ��H2CO3��
��3��������SO2����ͨ��Na2CO3��Һ�з�Ӧ����̼�����ƺ��������ƣ���Ӧ�Ļ�ѧ����ʽΪ��SO2+H2O+2Na2CO3=2NaHCO3+Na2SO3��
�ʴ�Ϊ��SO2+H2O+2Na2CO3=2NaHCO3+Na2SO3��
��4��Na2CO3��ǿ�������Σ�CO32-ˮ�����Һ�ʼ��ԣ�ˮ�����ӷ���ʽΪ��CO32-+H2O?HCO3-+OH-��
ƽ�ⳣ��K=$\frac{c��O{H}^{-}��c��HC{{O}_{3}}^{-}��}{c��C{{O}_{3}}^{2-}��}$=$\frac{c��O{H}^{-}��c��HC{{O}_{3}}^{-}��}{c��C{{O}_{3}}^{2-}��}$��$\frac{c��{H}^{+}��}{c��{H}^{+}��}$=$\frac{Kw}{K{a}_{2}}$=$\frac{1{0}^{-14}}{4.7��1{0}^{-11}}$=2.13��10-4��
�ʴ�Ϊ��2.13��10-4��
���� ���⿼����������ʵ���ƽ��Ӱ�����ء�����ˮ�⡢ƽ�ⳣ������ȣ����ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�

 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д�| A�� | ������Һ��������̼��īˮ���ɷ������������ | |
| B�� | ������ˮʱ�����˻�ѧ�������仯������ɱ�������������� | |
| C�� | ���ͷ����Ҫ�ɷ�������غ����ʣ��ֱ����ڵ���ʺͷǵ���� | |
| D�� | ��������Һ�м���CuSO4��Һ���г��������������ʿ����ڵ����ʵķ������ᴿ |
| A�� | Cu��Mg | B�� | Mg��Al | C�� | Al �� Si | D�� | SiO2��Zn |
| A�� | ��̭�ͽ�ֹ�Ʊ공������Ⱦ�ŷų�������·��ʻ���ɼ����������� | |
| B�� | ú�ĸ���Һ����������Ϊ��ѧ�仯 | |
| C�� | �������Ҵ����������Ƶ�������������ɱ�����÷��ز��� | |
| D�� | ��������������Դ���滯ʯȼ�ϣ������й������绷���յ�����--��������ɫ��� |
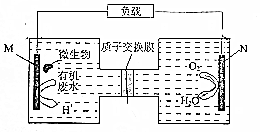 ��������ָ������������½���ѧ��ת��Ϊ���ܵ�װ�ã���ͼ������һ�����ォ�л���ˮ�е�����[CO��NH2��3]ת��Ϊ�Ի��������ʵ�װ�ã���������������ǣ�������
��������ָ������������½���ѧ��ת��Ϊ���ܵ�װ�ã���ͼ������һ�����ォ�л���ˮ�е�����[CO��NH2��3]ת��Ϊ�Ի��������ʵ�װ�ã���������������ǣ�������| A�� | M�缫��CO2��N2���� | B�� | H+�����ӽ���Ĥ���������ƶ� | ||
| C�� | ����ٽ��˷�Ӧ�е��ӵ�ת�� | D�� | N�缫��ӦʽΪ��O2+2H2O+4e-�T4OH- |
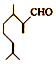 ����һ����Ҫ�����ϣ�������������������ɶ�������ױ���
����һ����Ҫ�����ϣ�������������������ɶ�������ױ��� �� �����й���Ҷȩ���������ױ���������ȷ���ǣ�������
�� �����й���Ҷȩ���������ױ���������ȷ���ǣ�������| A�� | ����Ϊͬ���칹�� | |
| B�� | ���߾�������ˮ�����ӳɷ�Ӧ | |
| C�� | ��Ҷȩ��һ��ͬ���칹������Ƿ��㴼 | |
| D�� | ��������ױ��ķ���ʽΪC10H14 |
 +
+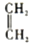 $\stackrel{��}{��}$
$\stackrel{��}{��}$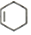
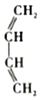
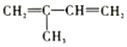 ��������2-��-1��3-����ϩ��
��������2-��-1��3-����ϩ�� b��
b�� c��
c��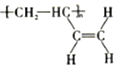
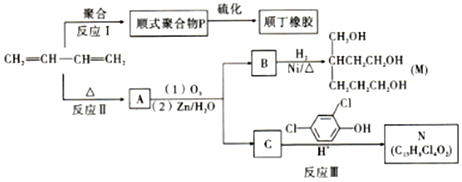
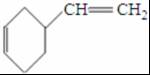 ����ӦIII�Ļ�ѧ����ʽ��
����ӦIII�Ļ�ѧ����ʽ��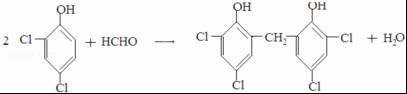 ��1molB��ȫת����M������H2��������6g��
��1molB��ȫת����M������H2��������6g��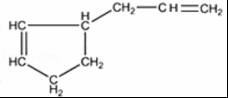 ��
��