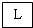题目内容
向盛有FeCl3溶液的试管中滴加少量氢氧化钠,溶液的现象为 ,所发生反应的方程式为 当生成物颜色不再变化后,再向试管中中加入足量HCl现象为 ,所发生反应的离子方程式为 .
考点:化学方程式的书写,离子方程式的书写,铁的氧化物和氢氧化物
专题:元素及其化合物
分析:FeCl3溶液的试管中滴加少量氢氧化钠,发生FeCl3+3NaOH=Fe(OH)3↓+3NaCl,加入盐酸,氢氧化铁与盐酸反应生成氯化铁,溶液变为黄色,以此解答.
解答:
解:向盛有FeCl3溶液的试管中滴加少量氢氧化钠,发生FeCl3+3NaOH=Fe(OH)3↓+3NaCl,溶液颜色变浅,生成红褐色沉淀,当生成物颜色不再变化后,再向试管中中加入足量HCl,沉淀溶解,发生反应的离子方程式为,
故答案为:溶液颜色变浅,生成红褐色沉淀;FeCl3+3NaOH=Fe(OH)3↓+3NaCl;沉淀溶解;Fe(OH)3+3H+=3Fe3++3H2O.
故答案为:溶液颜色变浅,生成红褐色沉淀;FeCl3+3NaOH=Fe(OH)3↓+3NaCl;沉淀溶解;Fe(OH)3+3H+=3Fe3++3H2O.
点评:本题综合考查铁的化合物的性质,为高频考点,侧重离子方程式和化学方程式的书写,注意物质的性质以及反应现象,难度不大.

练习册系列答案
 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
设NA为阿伏伽德罗常数.下列叙述正确的是( )
| A、20mL10mol?L-1浓硫酸或浓硝酸与足量铜加热反应转移电子数均为0.2NA |
| B、0.1mol的白磷(P4)或甲烷中所含的共价键数均为0.4NA |
| C、标准状况下,2.24L CI2通入足量H2O或NaOH溶液中转移的电子数均为0.1NA |
| D、在精炼铜或电镀铜的过程中,当阴极析出铜32g转移电子数为NA |
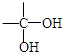
有机物A的分子式为C3H6O2,水解后得到一元酸M和一元醇N,已知M、N的相对分子质量相等,则下列叙述中不正确的是( )
| A、M中没有甲基? |
| B、A的属于酯的同分异构体还有一种 |
| C、N、M均不能发生银镜反应 |
| D、N分子中含有甲基? |
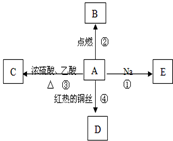 A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应.B物质中含有碳元素.
A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应.B物质中含有碳元素.

 在不同温度下的水溶液中c(H+)=10x mol/L,c(OH-)=10y mol/L,x与y的关系如图所示.请回答下列问题:
在不同温度下的水溶液中c(H+)=10x mol/L,c(OH-)=10y mol/L,x与y的关系如图所示.请回答下列问题: