题目内容
某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数.
(1)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g)
实验测得不同温度下的平衡数据列于下表:
(1)可以判断该分解反应已经达到平衡的是
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
(2)该分解反应的平衡常数表达式为 ,根据表中数据,列式计算25.0℃时的分解平衡常数: .(保留两位有效数字)
(3)取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0℃下达到分解平衡.若在恒温下压缩容器体积,氨基甲酸铵固体的质量 (填“增加”“减少”或“不变”);
(4)氨基甲酸铵分解反应的焓变△H 0(填“>”“=”或“<”),熵变△S 0 (填“>”“=”或“<”).此反应在该温度下能自发进行原因是 效应大于 效应.
(1)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g)
实验测得不同温度下的平衡数据列于下表:
| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压 强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体 总浓度/ mol?L-1 | 2.4× 10-3 | 3.4× 10-3 | 4.8× 10-3 | 6.8× 10-3 | 9.4× 10-3 |
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
(2)该分解反应的平衡常数表达式为
(3)取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0℃下达到分解平衡.若在恒温下压缩容器体积,氨基甲酸铵固体的质量
(4)氨基甲酸铵分解反应的焓变△H
考点:化学平衡常数的含义
专题:化学平衡专题
分析:(1)反应到达平衡状态时,正逆反应速率相等,平衡时各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,由此进行判断;
(2)化学平衡常数K=
,固体和纯溶剂不列入表达式中,并根据平衡数据来计算;
(3)根据压强对化学平衡移动的影响来回答判断;
(4)根据温度对化学平衡移动的影响以及反应前后气体量的变化来确定焓变和熵变的符号,该温度下能自发进行原因是△G<0.
(2)化学平衡常数K=
| 各个生成物平衡浓度系数次方的乘积 |
| 各个反应物平衡浓度系数次方的乘积 |
(3)根据压强对化学平衡移动的影响来回答判断;
(4)根据温度对化学平衡移动的影响以及反应前后气体量的变化来确定焓变和熵变的符号,该温度下能自发进行原因是△G<0.
解答:
解:(1)A.2v(NH3)═v(CO2),不能说明正逆反应速率相等,不一定是平衡状态,故A错误;
B.反应是一个前后系数和变化的反应,密闭容器中总压强不变,证明达到了平衡状态,故B正确;
C.密闭容器中混合气体的密度ρ=
,质量不守恒,分子变化,V不变,容器中总密度不变,证明达到了平衡状态,故C正确;
D.密闭容器中氨气的体积分数不变,不能证明达到平恒状态,故D错误.
故选BC;
(2)反应NH2COONH4(s)?2NH3(g)+CO2(g)的K=c2(NH3)?c(CO2),设二氧化碳浓度的变化量x,
NH2COONH4(s)?2NH3(g)+CO2(g)
初始浓度:0 0
变化浓度:2x x
平衡浓度:2x x
则3x=4.8×10-3mol/L,即x=1.6×10-3mol/L,K=1.6×10-3mol/L×(3.2×10-3)2≈1.6×10-8(mol?L-1)3,
故答案为:c2(NH3)?c(CO2);1.6×10-8(mol?L-1)3;
(3)若在恒温下压缩容器体积,则会将压强增大,平衡向左移动,固体质量增大,故答案为:增加;
(4)根据表中的数据分析:温度越高,则平衡气体的总浓度越大,所以升高温度,平衡正向移动,反应是吸热的,反应物是固体,产物是气体,该反应是熵增加的过程,即△H>0,△S>0,该温度下能自发进行原因是△G<0,即熵变量大于焓变量,故答案为:>;>;熵;焓.
B.反应是一个前后系数和变化的反应,密闭容器中总压强不变,证明达到了平衡状态,故B正确;
C.密闭容器中混合气体的密度ρ=
| m |
| V |
D.密闭容器中氨气的体积分数不变,不能证明达到平恒状态,故D错误.
故选BC;
(2)反应NH2COONH4(s)?2NH3(g)+CO2(g)的K=c2(NH3)?c(CO2),设二氧化碳浓度的变化量x,
NH2COONH4(s)?2NH3(g)+CO2(g)
初始浓度:0 0
变化浓度:2x x
平衡浓度:2x x
则3x=4.8×10-3mol/L,即x=1.6×10-3mol/L,K=1.6×10-3mol/L×(3.2×10-3)2≈1.6×10-8(mol?L-1)3,
故答案为:c2(NH3)?c(CO2);1.6×10-8(mol?L-1)3;
(3)若在恒温下压缩容器体积,则会将压强增大,平衡向左移动,固体质量增大,故答案为:增加;
(4)根据表中的数据分析:温度越高,则平衡气体的总浓度越大,所以升高温度,平衡正向移动,反应是吸热的,反应物是固体,产物是气体,该反应是熵增加的过程,即△H>0,△S>0,该温度下能自发进行原因是△G<0,即熵变量大于焓变量,故答案为:>;>;熵;焓.
点评:本题涉及化学平衡的判断、化学平衡常数的计算、化学平衡的移动等知识,属于综合知识的考查,难度不大.

练习册系列答案
相关题目
在锌与盐酸的反应中,HCl( )
| A、发生氧化反应 | B、是还原剂 |
| C、是氧化剂 | D、表现还原性 |
已知:CH4(g)+2O2(g)→CO2(g)+2H2O(l)+890kJ、CO(g)+
O2(g)→CO2(g)+282.5kJ.标准情况下,由CH4、CO、CO2组成的混合气体89.6L完全燃烧时能放出1010kJ的热量,并生成18g液体水,则燃烧前混合气体中CO占的体积分数为( )
| 1 |
| 2 |
| A、50% | B、60% |
| C、70% | D、80% |
下列水解离子方程式正确的是( )
| A、CH3COO-+H2O?CH3COOH+OH- |
| B、NH4++H2O?NH4OH+H+ |
| C、Fe3++H2O?Fe(OH)3+H+ |
| D、Al3++3HCO3-═Al(OH)3↓+3CO2↑ |
下列物质为纯净物的是( )
| A、冰醋酸 | B、医用酒精 |
| C、福尔马林 | D、汽油 |



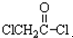 与足量的NaOH溶液共热充分反应的化学方程式:
与足量的NaOH溶液共热充分反应的化学方程式: