题目内容
在20℃时,氯化钠的溶解度为36g,取一定量该温度下的饱和氯化钠溶液用惰性电极进行电解.当阳极产生气体为11.2L(标准状况)时,氯化钠完全电解,所得溶液的密度为1.2g/mL.试计算:
(1)电解时所取饱和氯化钠溶液的质量.
(2)电解后溶液中溶质的物质的量浓度.
(1)电解时所取饱和氯化钠溶液的质量.
(2)电解后溶液中溶质的物质的量浓度.
考点:电解原理
专题:电化学专题
分析:(1)根据溶解度计算质量分数,根据电解产生的氯气的量计算溶质氯化钠的质量,进而计算溶液质量;
(2)根据电解方程式结合氯气的量计算氢氧化钠的量,根据公式c=
计算物质的量浓度.
(2)根据电解方程式结合氯气的量计算氢氧化钠的量,根据公式c=
| n |
| V |
解答:
解:(1)用惰性电极进行电解饱和氯化钠溶液,当阳极析出11.2L即0.5mol气体(标准状况)时,阳极上是氯离子失电子,电极反应为:2Cl--2e-═Cl2↑,所以放电的氯离子是1mol,氯化钠的物质的量是1mol,质量是58.5g,该温度下的饱和溶液的质量分数=
×100%=
,所取饱和食盐水的质量=
=221g,
答:电解时,所取饱和食盐水的质量是221g;
(2)2NaCl+2H2O
2NaOH+Cl2↑+H2↑,当阳极析出11.2L即0.5mol氯气(标准状况)时,生成氢氧化钠1mol,溶液的体积V=
=
=0.184L,
电解后溶液中NaOH的物质的量浓度c=
≈5.4mol/L,答:电解后溶液中NaOH的物质的量浓度为5.4mol/L;
| 36g |
| 136g |
| 9 |
| 34 |
| 58.5g | ||
|
答:电解时,所取饱和食盐水的质量是221g;
(2)2NaCl+2H2O
| ||
| m |
| ρ |
| 221g |
| 1200g/L |
电解后溶液中NaOH的物质的量浓度c=
| 1mol |
| 0.184L |
点评:本题涉及电解池的工作原理、质量分数的计算方法知识,属于综合知识的考查题,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
蛋白质受某些理化因素的影响,其空间结构发生变化,引起理化性质和生物活性的变化,称为蛋白质的( )
| A、水解 | B、盐析 | C、变性 | D、聚沉 |
1-氯丙烷和2-氯丙烷分别与NaOH乙醇溶液共热的反应( )
| A、产物相同 |
| B、反应类型不同 |
| C、碳氢键断裂位置相同 |
| D、都属于取代反应 |
下列说法中不正确的是( )
| A、实验室制Fe(OH)2时应将汲有NaOH溶液的胶头滴管伸入FeSO4溶液液面下,缓缓挤出碱液 |
| B、镁铝合金的硬度和熔点都比纯铝和纯镁大 |
| C、结晶形和无定形二氧化硅统称硅石 |
| D、常温下,铝能和空气里的氧气反应生成一层致密的氧化膜,从而常温耐腐蚀 |
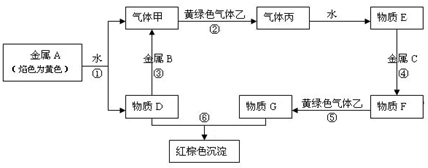
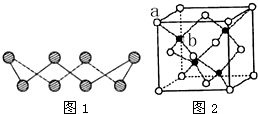 ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:
ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题: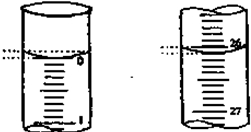
 某学生用物质的量的浓度为a mol/L的标准NaOH去测定V mL HCl溶液的物质的量浓度.用甲基橙作指示剂. 回答下列问题:
某学生用物质的量的浓度为a mol/L的标准NaOH去测定V mL HCl溶液的物质的量浓度.用甲基橙作指示剂. 回答下列问题: