题目内容
4.下列有关一定物质的量浓度溶液的配制说法正确的是( )| A. | 将固体加入容量瓶中溶解并稀释至刻度线,配制成一定物质的量浓度的溶液 | |
| B. | 稀释硫酸时,往装有浓硫酸的烧杯中注入水 | |
| C. | 用托盘天平称取10.600 g的Na2CO3固体,溶于1 L的水可配成0.1 mol/L的溶液 | |
| D. | 容量瓶中残留少量蒸馏水时,无需干燥,对配制的结果没有影响 |
分析 A.依据容量瓶使用注意事项解答;
B.浓硫酸稀释应将浓硫酸加入到水中;
C.托盘天平精确值为0.1g;
D.分析操作对溶质的物质的量n和对溶液体积V的影响,依据c=$\frac{n}{V}$进行分析解答.
解答 解:A.容量瓶为精密仪器,不能用来稀释溶液、溶解固体,故A错误;
B.浓硫酸稀释应将浓硫酸加入到水中,并用玻璃棒不断搅拌,故B错误;
C.托盘天平精确值为0.1g,所以不能用托盘天平称取10.600 g的Na2CO3固体,故C错误;
D.容量瓶中残留少量蒸馏水时,对溶质的物质的量n和对溶液体积V都不产生影响,溶液浓度不变,故D正确;
故选:D.
点评 本题考查了一定物质的量浓度溶液的配制,明确容量瓶构造及使用方法和注意问题,熟悉浓硫酸稀释的正确操作是解题关键,题目难度不大.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
17.甲原子与乙原子的质量比为a:b,而乙原子与碳12 原子的质量比为c:d,则甲原子的相对原子质量为( )
| A. | $\frac{12ac}{bd}$ | B. | $\frac{bc}{12ac}$ | C. | $\frac{12bd}{ac}$ | D. | $\frac{ab}{12bc}$ |
15.下列叙述正确的是( )
| A. | NaHSO4固体融化时破坏的是离子键 | |
| B. | 含有共价键的化合物都是共价化合物 | |
| C. | Na2O溶于水时只破坏离子键没破坏共价键 | |
| D. | 强电解质都是离子化合物 |
12.现有三组液体:①氯化钠溶液和四氯化碳组成的混合液 ②43%的乙醇溶液 ③氯化钠和单质碘的水溶液,分离以上各混合液的正确方法依次是( )
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
16.对于常温下pH为1的硝酸溶液,下列叙述不正确的是( )
| A. | 该溶液1 mL稀释至100 mL后,pH等于3 | |
| B. | 向该溶液中加入等体积、pH为13的氢氧化钡溶液恰好完全中和 | |
| C. | 该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为10-12 | |
| D. | 该溶液中水电离出的c(H+)是pH为3的硝酸中水电离出的c(H+)的100倍 |
13.下列溶液一定呈中性的是( )
| A. | c(H+)=1×10-7mol/L的溶液 | |
| B. | 非电解质溶于水得到的溶液 | |
| C. | 酸与碱恰好完全反应生成正盐的溶液 | |
| D. | c 2(H+)=Kw |
13.下列关于镁铝化学性质的表述不正确的是( )
| 铝 | 镁 | |
| A.与非金属反应 | 能被Cl2、O2氧化 | 能与N2、O2反应 |
| B.与水反应 | 常温下难与水反应 | 常温下能与水缓慢反应 |
| C.与碱反应 | 能溶于碱溶液 | 能溶于碱溶液 |
| D.与某些氧化物反应 | 能与Fe2O3、MnO2、C如O3等金属氧化物发生铝热反应 | 能在CO2中燃烧 |
| A. | A | B. | B | C. | C | D. | D |
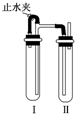 实验室制备Fe(OH)2沉淀时,由于其在空气中极易发生反应4Fe(OH)2+O2+2H2O=4Fe(OH)3.(填化学方程式)而很难观察到沉淀的颜色.为制得Fe(OH)2白色沉淀,有人设计了如图所示的装置,用NaOH溶液、铁屑、稀H2SO4等试剂制备.实验时试管Ⅰ里应加入稀H2SO4和铁屑(填试剂名称).在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是检验试管Ⅱ出口处排出的H2的纯度,当排出的H2已经纯净时再夹紧止水夹.
实验室制备Fe(OH)2沉淀时,由于其在空气中极易发生反应4Fe(OH)2+O2+2H2O=4Fe(OH)3.(填化学方程式)而很难观察到沉淀的颜色.为制得Fe(OH)2白色沉淀,有人设计了如图所示的装置,用NaOH溶液、铁屑、稀H2SO4等试剂制备.实验时试管Ⅰ里应加入稀H2SO4和铁屑(填试剂名称).在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是检验试管Ⅱ出口处排出的H2的纯度,当排出的H2已经纯净时再夹紧止水夹.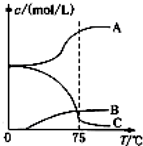 氯酸钠(NaClO3)是无机盐工业的重要产品之一.
氯酸钠(NaClO3)是无机盐工业的重要产品之一.