题目内容
氧化还原反应的实质是( )
| A、得到氧元素与失去氧元素 |
| B、有无新物质生成 |
| C、化合价的升降 |
| D、电子的得失或共用电子对的偏移 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:氧化还原反应的实质为电子转移,特征为化合价的升降,以此来解答.
解答:
解:氧化还原反应的实质为电子的转移(电子的得失或偏移),化合价的升降为特征,而有无新物质生成不一定有化合价的变化,氧原子的得失也为特征,
故选D.
故选D.
点评:本题较简单,考查氧化还原反应的实质,注意特征和实质的差别,明确宏观与微观的不同即可解答,题目难度不大.

练习册系列答案
相关题目
关于Cl-的说法正确的是( )
| A、Cl-呈黄绿色 |
| B、Cl-有毒 |
| C、Cl-具有氧化性 |
| D、Cl-是稳定结构 |
已知:2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ?mol-12CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452kJ?mol-1H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ?mol-1下列说法正确的是( )
| A、H2(g)的燃烧热为571.6 kJ?mol-1 | ||||||
| B、同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 | ||||||
C、
| ||||||
| D、3H2(g)+CO2(g)=CH3OH(l)+H2O(l)△H=+135.9 kJ?mol-1 |
要配制浓度约为2mol/LNaOH溶液100mL,下面的操作正确的是( )
| A、用托盘天平称取8gNaOH固体(NaOH固体放置于天平的托盘上),放入250mL烧杯中,用100mL量筒量取100mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解 |
| B、称取8gNaOH固体,放入100mL量筒中,边搅拌边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100mL |
| C、称取8gNaOH固体,放入100mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀 |
| D、用50mL量筒量取40mL5mol/LNaOH溶液,倒入100mL容量瓶中,然后加蒸馏水定容直至刻度线,盖好瓶塞,反复摇匀,装瓶就行 |
人体中正常的血红蛋白中含有Fe2+,若误食亚硝酸盐,则导致血红蛋白中的Fe2+转化高铁(Fe3+)血红蛋白而中毒,服用维生素C可解除亚硝酸盐中毒.下列叙述中正确的是( )
| A、亚硝酸盐是还原剂 |
| B、维生素C发生还原反应 |
| C、维C将Fe3+转化成Fe2+ |
| D、亚硝酸盐被氧化 |
实验室里需用495mL 0.1mol/L的硫酸铜溶液,以下操作正确的是( )
| A、称取7.68 g硫酸铜,加入500 mL水 |
| B、称取12.5 g胆矾配成500 mL溶液 |
| C、称取8.0 g硫酸铜,加入500 mL水 |
| D、称取12.0 g胆矾配成500 mL溶液 |
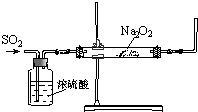 同学们利用如图装置探究SO2与Na2O2的反应.
同学们利用如图装置探究SO2与Na2O2的反应.