题目内容
亚氯酸盐(NaClO2)可用作漂白剂,在常温下不见光时可保存一年,但在酸性溶液中因生成亚氯酸而发生分解:5HClO2==4ClO2 +H++Cl-+2H2O分解时,刚加入硫酸时反应缓慢,随后突然反应释放出ClO2,这是因为( )
A.酸使亚氯酸的氧化性增强 B.溶液中的H+起催化作用
C.溶液中的Cl-起催化作用 D.逸出的ClO2使反应的生成物浓度降低
C
【解析】试题分析:反应刚开始减慢,是由于反应中加入了H+,但是反应开始后有Cl-的生成,反应迅速加快,所以选C。
考点:影响化学反应的速率
点评:通过已知条件判断影响反应速率的快慢,要注意反应中参与反应的离子,才能更好的解决问题。

| |||||||||||||||||||
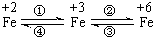 亚铁盐、铁盐、高铁酸盐等铁的重要化合物之间可以相互转化(见图).利用转化过程中发生的特征变化,不仅能够实现物质或能量的转化,还用于化学的定性或定量研究.
亚铁盐、铁盐、高铁酸盐等铁的重要化合物之间可以相互转化(见图).利用转化过程中发生的特征变化,不仅能够实现物质或能量的转化,还用于化学的定性或定量研究.