��Ŀ����
��ȸʯ����Ҫ�ɷ�ΪCuCO3?Cu��OH��2��ijͬѧ��ƴӿ�ȸʯ��ұ��ͭ�ķ������£�
��1������1�������뽹̿һ����ȣ���������ͭ��������̼��ˮ��
�÷�Ӧ�Ļ�ѧ����ʽ��
��2������2������m g��ȸʯ������1������ȸʯ�����ӹ���ϡ�������2�����ˣ�����Һ�ֳ����ȷݣ�
��д����ȸʯ��ϡ�����ܽ�����ӷ���ʽ
���ڹ��˲����б����õ��IJ������������ձ�������������Ҫ ��
����һ���м���������ۣ����ͭ��
�ۼ������ۺ�õ���ͭ�к��еĹ���������Ҫ�� ����ȥͭ�и����ʵļ�����
�ܸ���Һ�����۷�Ӧ�������� ��
��ijͬѧֱ�Ӱ���Һ����Ƭ������Ƴ�ԭ�������ȡͭ���为�������ĵ缫����ʽ ��
����һ�������ⶨ��ȸʯ��ͭ�ĺ������������£�
a������Һ�м�������KI�������ķ�ӦΪ��2Cu2++4I-=2CuI+I2
b�� �Ե���Ϊָʾ������Na2S2O3��Һ�ⶨ���ɵ� I2��
�����ķ�ӦΪ��I2+2S2O32-=2I-+S2O62-
��ȥ2.0��10-3mol/L��Na2S2O3��ҺV L������Һ����ɫ����ɫ��Ϊ ɫ��������Ӳ��ָ�ʱ��˵����Ӧǡ����ȫ����������ʵ�飬��ÿ�ȸʯ��ͭ���������� ���Ժ�m��V�Ĵ���ʽ��ʾ��
��1������1�������뽹̿һ����ȣ���������ͭ��������̼��ˮ��
�÷�Ӧ�Ļ�ѧ����ʽ��
��2������2������m g��ȸʯ������1������ȸʯ�����ӹ���ϡ�������2�����ˣ�����Һ�ֳ����ȷݣ�
��д����ȸʯ��ϡ�����ܽ�����ӷ���ʽ
���ڹ��˲����б����õ��IJ������������ձ�������������Ҫ
����һ���м���������ۣ����ͭ��
�ۼ������ۺ�õ���ͭ�к��еĹ���������Ҫ��
�ܸ���Һ�����۷�Ӧ��������
��ijͬѧֱ�Ӱ���Һ����Ƭ������Ƴ�ԭ�������ȡͭ���为�������ĵ缫����ʽ
����һ�������ⶨ��ȸʯ��ͭ�ĺ������������£�
a������Һ�м�������KI�������ķ�ӦΪ��2Cu2++4I-=2CuI+I2
b�� �Ե���Ϊָʾ������Na2S2O3��Һ�ⶨ���ɵ� I2��
�����ķ�ӦΪ��I2+2S2O32-=2I-+S2O62-
��ȥ2.0��10-3mol/L��Na2S2O3��ҺV L������Һ����ɫ����ɫ��Ϊ
���㣺ͭ����������Ҫ���������Ҫ����,̽�����ʵ���ɻ�������ʵĺ���
ר�⣺ʵ����,������Ҫ�Ľ������仯����
��������1����ȸʯ�뽹̿һ����ȣ����ȷ����ֽ⣺CuCO3?Cu��OH��2
2CuO+CO2��+H2O�����ý�̿��ԭ������2CuO+C
2Cu+CO2���������ܷ�ӦΪ
CuCO3?Cu��OH��2+C
2Cu+2CO2��+H2O��
��2���ٿ�ȸʯ��ϡ���ᷴӦ��CuCO3?Cu��OH��2+4H2SO4=2CuSO4+CO2��+3H2O�����ӷ���ʽΪ��CuCO3?Cu��OH��2+4H+=2Cu2++CO2��+3H2O��
���ڹ��˲����б����õ��IJ������������ձ�������������Ҫ©����
����һ���м���������ۣ����ͭ����Ϊ���������Եõ���ͭ�к��еĹ���������Ҫ�ǹ��������ۣ���ȥͭ�и����ʵļ����ǽ�����Ͷ��������ϡ�����ϡ�����г�ַ�Ӧ����ˣ�
������Һ�м������ۣ�CuSO4��H2SO4���������۷�Ӧ��CuSO4+Fe=Cu+FeSO4��H2SO4+Fe=H2��+FeSO4��
�ݰ���Һ����Ƭ������Ƴ�ԭ��أ�����������ԭ��Һ�е�ͭ���ӣ��������Ǹ�������ӦΪ��Fe-2e-=Fe2+��
���ݷ���ʽ������ϵʽ��Cu2+��S2O32��Ȼ�����ͭԪ�ص������������������ٷ�����
| ||
| ||
CuCO3?Cu��OH��2+C
| ||
��2���ٿ�ȸʯ��ϡ���ᷴӦ��CuCO3?Cu��OH��2+4H2SO4=2CuSO4+CO2��+3H2O�����ӷ���ʽΪ��CuCO3?Cu��OH��2+4H+=2Cu2++CO2��+3H2O��
���ڹ��˲����б����õ��IJ������������ձ�������������Ҫ©����
����һ���м���������ۣ����ͭ����Ϊ���������Եõ���ͭ�к��еĹ���������Ҫ�ǹ��������ۣ���ȥͭ�и����ʵļ����ǽ�����Ͷ��������ϡ�����ϡ�����г�ַ�Ӧ����ˣ�
������Һ�м������ۣ�CuSO4��H2SO4���������۷�Ӧ��CuSO4+Fe=Cu+FeSO4��H2SO4+Fe=H2��+FeSO4��
�ݰ���Һ����Ƭ������Ƴ�ԭ��أ�����������ԭ��Һ�е�ͭ���ӣ��������Ǹ�������ӦΪ��Fe-2e-=Fe2+��
���ݷ���ʽ������ϵʽ��Cu2+��S2O32��Ȼ�����ͭԪ�ص������������������ٷ�����
���
�⣺��1����ȸʯ�뽹̿һ����ȣ����ȷ����ֽ⣺CuCO3?Cu��OH��2
2CuO+CO2��+H2O�����ý�̿��ԭ������2CuO+C
2Cu+CO2���������ܷ�ӦΪ
CuCO3?Cu��OH��2+C
2Cu+2CO2��+H2O���ʴ�Ϊ��CuCO3?Cu��OH��2+C
2Cu+2CO2��+H2O��
��2���ٿ�ȸʯ��ϡ���ᷴӦ��CuCO3?Cu��OH��2+4H2SO4=2CuSO4+CO2��+3H2O�����ӷ���ʽΪ��CuCO3?Cu��OH��2+4 H+=2Cu2++CO2��+3H2O��
�ʴ�Ϊ��CuCO3?Cu��OH��2+4 H+=2Cu2++CO2��+3H2O��
���ڹ��˲����б����õ��IJ������������ձ�������������Ҫ©�����ʴ�Ϊ��©����
����һ���м���������ۣ����ͭ����Ϊ���������Եõ���ͭ�к��еĹ���������Ҫ�ǹ��������ۣ���ȥͭ�и����ʵļ����ǽ�����Ͷ��������ϡ�����ϡ�����г�ַ�Ӧ����ˣ��ʴ�Ϊ�����ۣ�������Ͷ��������ϡ�����ϡ�����г�ַ�Ӧ����ˣ����ô������������ɣ���
������Һ�м������ۣ�CuSO4��H2SO4���������۷�Ӧ��CuSO4+Fe=Cu+FeSO4��H2SO4+Fe=H2��+FeSO4�������۷�Ӧ��������Cu2+��H+���ʴ�Ϊ��Cu2+��H+��
�ݰ���Һ����Ƭ������Ƴ�ԭ��أ�����������ԭ��Һ�е�ͭ���ӣ��������Ǹ�������ӦΪ��Fe-2e-=Fe2+���ʴ𰸣�Fe-2e-=Fe2+��
�������۱���ɫ����ѡ�������ָʾ��������Һ����ɫ��Ϊ��ɫ���Ұ������ɫ���ٱ仯˵���ζ������յ㣬
Cu2+��S2O32
1 1
n��Cu2+�� 2.0��10-3mol/L��VL��
n��Cu2+��=2.0��10-3Vmol��ͭ������2.0��10-3Vmol��64g/mol=128��10-3Vg������mg��ȸʯ���ӹ�����ϡ���Ὣ���ܽ⣬���ˣ�����Һ�ֳ����ȷݣ�����һ����Һ�к���
��ȸʯ�����Բ�ÿ�ȸʯ��ͭ������������
��100%=
��100%��
�ʴ�Ϊ���ޣ�
��100%��
| ||
| ||
CuCO3?Cu��OH��2+C
| ||
| ||
��2���ٿ�ȸʯ��ϡ���ᷴӦ��CuCO3?Cu��OH��2+4H2SO4=2CuSO4+CO2��+3H2O�����ӷ���ʽΪ��CuCO3?Cu��OH��2+4 H+=2Cu2++CO2��+3H2O��
�ʴ�Ϊ��CuCO3?Cu��OH��2+4 H+=2Cu2++CO2��+3H2O��
���ڹ��˲����б����õ��IJ������������ձ�������������Ҫ©�����ʴ�Ϊ��©����
����һ���м���������ۣ����ͭ����Ϊ���������Եõ���ͭ�к��еĹ���������Ҫ�ǹ��������ۣ���ȥͭ�и����ʵļ����ǽ�����Ͷ��������ϡ�����ϡ�����г�ַ�Ӧ����ˣ��ʴ�Ϊ�����ۣ�������Ͷ��������ϡ�����ϡ�����г�ַ�Ӧ����ˣ����ô������������ɣ���
������Һ�м������ۣ�CuSO4��H2SO4���������۷�Ӧ��CuSO4+Fe=Cu+FeSO4��H2SO4+Fe=H2��+FeSO4�������۷�Ӧ��������Cu2+��H+���ʴ�Ϊ��Cu2+��H+��
�ݰ���Һ����Ƭ������Ƴ�ԭ��أ�����������ԭ��Һ�е�ͭ���ӣ��������Ǹ�������ӦΪ��Fe-2e-=Fe2+���ʴ𰸣�Fe-2e-=Fe2+��
�������۱���ɫ����ѡ�������ָʾ��������Һ����ɫ��Ϊ��ɫ���Ұ������ɫ���ٱ仯˵���ζ������յ㣬
Cu2+��S2O32
1 1
n��Cu2+�� 2.0��10-3mol/L��VL��
n��Cu2+��=2.0��10-3Vmol��ͭ������2.0��10-3Vmol��64g/mol=128��10-3Vg������mg��ȸʯ���ӹ�����ϡ���Ὣ���ܽ⣬���ˣ�����Һ�ֳ����ȷݣ�����һ����Һ�к���
| mg |
| 2 |
| 128��10 -3Vg | ||
|
| 256��10 -3V |
| m |
�ʴ�Ϊ���ޣ�
| 256��10 -3V |
| m |
���������⿼��������ԭ��Ӧ�ļ��㣬�����ʱע�ⷴӦ�����ԭ���ͷ���ʽ����д���������ʵ���Ӧ���ڻ�ѧ����ʽ�ļ�������Ŀ�ѶȲ���

��ϰ��ϵ�д�
�����Ŀ
��ͬ�¶ȣ������Ϊ0.5L���������������з������淴Ӧ��A��g��+3B��g���T2C��g����H=-92.6kJ?mol-1��ʵ���÷�Ӧ����ʼ���ﵽƽ��ʱ���й��������±���ʾ ������������ȷ���ǣ�������
| ������� | ������������/ | �ﵽƽ��ʱ��ϵ�����仯 | ||
| A | B | C | ||
| �� | 1 | 3 | 0 | ����46.3kJ |
| �� | 0.3 | 0.9 | 1.4 | |
| A����ƽ��ʱ������������C�����ʵ���Ũ�Ⱦ�Ϊ1.0mol?L-1 |
| B�������ٴ�ƽ��Aת������50% |
| C���������д�ƽ��ʱ���յ�����Ϊ18.52kJ |
| D������ʼ������A��B��C��Ϊ0.5mol�����ƽ��ǰ�ԣ��������ԣ��棩 |
��FeSO4��Fe2��SO4��3��CuSO4�Ļ����Һ600mL������c��SO42-��=0.1mol?L-1���ڻ��Һ��Ͷ��һЩп�ۣ���Ӧ��õ�һЩ������������ⶨ�����к���Cu��Fe��������Zn����Һ�л���0.01molFe2+���ݴ˿�֪Ͷ���п�������ǣ�������
| A��13g | B��9.75g |
| C��6.5g | D��3.25g |
ij��Һ��ֻ���ܺ������������еļ��֣���������Һ�к��Ľ��ٵ�H+��OH-����Na+��NH4+��SO42-��CO32-��NO3-��ȡ200mL����Һ����Ϊ����������ݷֱ�������ʵ�飮ʵ��1����һ�ݼ����������ռ���ȣ������������ڱ�״����Ϊ224mL��ʵ��2���ڶ����ȼ������������ᣬ�������ټ���������BaCl2��Һ���ù���2.33g������˵����ȷ���ǣ�������
| A������Һ��һ������Na+����c��Na+����0.1 mol?L-1 |
| B������Һ�п��ܺ���Na+ |
| C������Һ��һ������NO3- |
| D������Һ�п϶�����NH4+��SO42-��CO32-��NO3- |
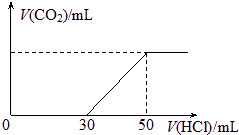 ����£���100 mL 0.1mol?L-1ijNaOH��Һ��ͨ��һ����CO2������������Һ�еμ�ijŨ�ȵ�ϡ���ᣬ�μ�������������������������ͼ��ʾ�����������ɵ�CO2ȫ���ݳ�������
����£���100 mL 0.1mol?L-1ijNaOH��Һ��ͨ��һ����CO2������������Һ�еμ�ijŨ�ȵ�ϡ���ᣬ�μ�������������������������ͼ��ʾ�����������ɵ�CO2ȫ���ݳ�������