题目内容
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | 浓硝酸在光照下颜色变黄 | 浓硝酸具有不稳定性 |
| B | 浓硫酸具有酸性和脱水性 | 浓硫酸可使PH试纸先变红后变黑 |
| C | Cl2和SO2均有漂白性 | Cl2和SO2均可使含有酚酞的NaOH溶液褪色 |
| D | C的还原性小于Si | 可用焦炭和石英在高温下反应制取粗硅和CO2 |
| A、A | B、B | C、C | D、D |
考点:硝酸的化学性质,氯气的化学性质,二氧化硫的化学性质,浓硫酸的性质
专题:元素及其化合物
分析:A.硝酸不稳定,见光易分解生成二氧化氮;
B.浓硫酸具有酸性,可使pH试纸变红,又由于浓硫酸具有脱水性,所以变红后又变黑;
C.Cl2与水反应生成次氯酸,次氯酸具有漂白性,能使指示剂褪色;二氧化硫是酸性氧化物,能与氢氧化钠反应生成亚硫酸钠和水,溶液的碱性减弱,颜色褪去;
D.焦炭和石英反应生成硅和一氧化碳气体,气体逸出,促使反应向正方向进行.
B.浓硫酸具有酸性,可使pH试纸变红,又由于浓硫酸具有脱水性,所以变红后又变黑;
C.Cl2与水反应生成次氯酸,次氯酸具有漂白性,能使指示剂褪色;二氧化硫是酸性氧化物,能与氢氧化钠反应生成亚硫酸钠和水,溶液的碱性减弱,颜色褪去;
D.焦炭和石英反应生成硅和一氧化碳气体,气体逸出,促使反应向正方向进行.
解答:
解:A.硝酸不稳定,见光易分解生成二氧化氮,二氧化氮溶于硝酸显黄色,故A正确;
B.浓硫酸具有酸性,可使pH试纸变红,又由于浓硫酸具有脱水性,所以变红后又变黑,故B正确;
C.Cl2与水反应生成次氯酸,次氯酸具有漂白性,能使指示剂褪色;SO2具有漂白性,但不能是指示剂褪色,二氧化硫是酸性氧化物,能与氢氧化钠反应生成亚硫酸钠和水,溶液的碱性减弱,颜色褪去,故C错误;
D.虽然碳的还原性小于Si,但高温下焦炭和石英反应生成硅和一氧化碳气体,气体逸出,促使反应向正方向进行,故可用焦炭和石英在高温下反应制取粗硅和CO2,故D错误;
故选AB.
B.浓硫酸具有酸性,可使pH试纸变红,又由于浓硫酸具有脱水性,所以变红后又变黑,故B正确;
C.Cl2与水反应生成次氯酸,次氯酸具有漂白性,能使指示剂褪色;SO2具有漂白性,但不能是指示剂褪色,二氧化硫是酸性氧化物,能与氢氧化钠反应生成亚硫酸钠和水,溶液的碱性减弱,颜色褪去,故C错误;
D.虽然碳的还原性小于Si,但高温下焦炭和石英反应生成硅和一氧化碳气体,气体逸出,促使反应向正方向进行,故可用焦炭和石英在高温下反应制取粗硅和CO2,故D错误;
故选AB.
点评:本题侧重元素化合物性质的考查,是高频考点,把握硝酸、浓硫酸、氯气、二氧化硫、碳、硅的性质等是解题关键,综合性较强,题目难度不大.

练习册系列答案
相关题目
NA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A、1mol Cl2参加的任何反应转移电子数都是2NA |
| B、标准状况下,22.4mL水中含有的分子数目约为1.24NA |
| C、常温常压下,29g乙基(-C2H5)所含电子数为13NA |
| D、0.1mol Na2O2中含有离子总数为0.4NA |
下列实验操作能达到目的是( )
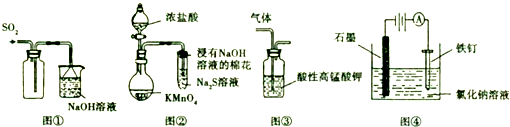

| A、可用图①所示装置收集SO2 |
| B、可用图②所示装置比较KMnO4、Cl2、S的氧化性强弱 |
| C、可用图③所示装置除去CH4中混有的少量C2H4 |
| D、可用图④所示装置防止铁钉生锈 |
下列图示与对应叙述相符合的是( )
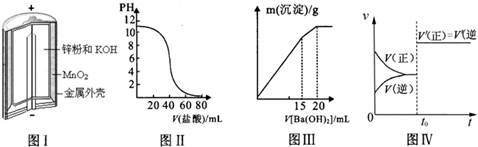

| A、图Ⅰ所示锌锰碱性电池正极的电极反应式为:MnO2+H2O+2e-═MnOOH+OH- |
| B、图Ⅱ表示盐酸滴加到0.1mol?L-1某碱溶液中得到的滴定曲线,由图Ⅱ可知二者恰 好中和时,所得溶液的pH>7 |
| C、图Ⅲ表示某明矾溶液中加入Ba(OH)2溶液时,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20mL Ba(OH)2溶液时,沉淀全部是BaSO4 |
| D、图Ⅳ表示已达平衡的某反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件一定是加入催化剂 |
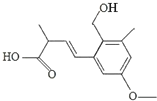 某有机物的结构简式如图,下列叙述正确的是( )
某有机物的结构简式如图,下列叙述正确的是( )| A、该有机物的分子式为C14H20O4 |
| B、该有机物能发生取代、加成和聚合反应 |
| C、1mol该有机物最多能与3mol NaOH反应 |
| D、该有机物分子中所有碳原子一定共平面 |
下列两组热化学方程式中,有关△H的比较正确的是( )
①CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H1
CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H2
②NaOH(aq)+
H2SO4(浓)═
Na2SO4(aq)+H2O(l);△H3
NaOH(aq)+CH3COOH(aq)═CH3COONa(aq)+H2O(l);△H4.
①CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H1
CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H2
②NaOH(aq)+
| 1 |
| 2 |
| 1 |
| 2 |
NaOH(aq)+CH3COOH(aq)═CH3COONa(aq)+H2O(l);△H4.
| A、△H1>△H2;△H3>△H4 |
| B、△H1>△H2;△H3<△H4 |
| C、△H1=△H2;△H3<△H4 |
| D、△H1<△H2;△H3>△H4 |
设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A、0.1mol NH3溶于足量水中(不考虑氨气挥发),溶液中N原子的数目为0.1NA |
| B、在常温下,若CO与CO2的体积相等,则它们的物质的量相等 |
| C、标准状况下,22.4L NO与CO2的混合气体中含有O的原子数为3NA |
| D、在常温常压下,22.4L氢气的质量为2g |
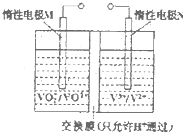 钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域.
钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域.