题目内容
下列各图示实验设计和操作合理的是( )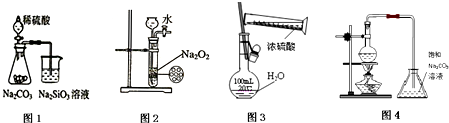

| A、图1 证明非金属性强弱:S>C>Si |
| B、图2 制备少量氧气 |
| C、图3 配制一定物质的量浓度的硫酸溶液 |
| D、图4 制备少量乙酸丁酯 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.发生强酸制取弱酸的反应;
B.过氧化钠为粉末固体;
C.不能在容量瓶中稀释浓硫酸;
D.反应物乙酸、1-丁醇的沸点低于产物乙酸丁酯的沸点.
B.过氧化钠为粉末固体;
C.不能在容量瓶中稀释浓硫酸;
D.反应物乙酸、1-丁醇的沸点低于产物乙酸丁酯的沸点.
解答:
解:A.发生强酸制取弱酸的反应可知最高价含氧酸的酸性为硫酸>碳酸>硅酸,可比较非金属性S>C>Si,故A正确;
B.过氧化钠为粉末固体,固体与液体接触后,不能分离,图中隔板不能用作粉末固体与液体的反应,故B错误;
C.不能在容量瓶中稀释浓硫酸,应在烧杯中稀释、冷却后转移到容量瓶中,故C错误;
D.反应物乙酸、1-丁醇的沸点低于产物乙酸丁酯的沸点,若采用图中装置,会造成反应物的大量挥发,大大降低了反应物的转化率,故D错误;
故选A.
B.过氧化钠为粉末固体,固体与液体接触后,不能分离,图中隔板不能用作粉末固体与液体的反应,故B错误;
C.不能在容量瓶中稀释浓硫酸,应在烧杯中稀释、冷却后转移到容量瓶中,故C错误;
D.反应物乙酸、1-丁醇的沸点低于产物乙酸丁酯的沸点,若采用图中装置,会造成反应物的大量挥发,大大降低了反应物的转化率,故D错误;
故选A.
点评:本题考查化学实验方案的评价,为高频考点,涉及非金属性比较、固液反应装置、溶液配制、乙酸丁酯制备等,把握物质的性质及反应原理为解答的关键,注意实验方案的评价性、操作性分析,选项D为解答的难点,题目难度不大.

练习册系列答案
 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
下列有关电子云和原子轨道的说法正确的是( )
| A、原子核外的电子像云雾一样笼罩在原子核周围,故称电子云 |
| B、s能级的原子轨道呈球形,处在该轨道上的电子只能在球壳内运动 |
| C、p能级的原子轨道呈哑铃形,随着能层的增加,p能级原子轨道也在增多 |
| D、电子云的伸展方向与能量是无关的 |
 一首脍炙人口的民歌《茉莉花》唱得沁人心脾,茉莉醛具有浓郁的茉莉花香,其结构简式如图所示.关于茉莉醛的下列叙述正确的是( )
一首脍炙人口的民歌《茉莉花》唱得沁人心脾,茉莉醛具有浓郁的茉莉花香,其结构简式如图所示.关于茉莉醛的下列叙述正确的是( )| A、茉莉醛与苯甲醛互为同系物 |
| B、在加热和催化剂作用下加氢,每摩尔茉莉醛最多能消耗3mol氢气 |
| C、一定条件下,茉莉醛能发生氧化、还原、酯化等反应 |
| D、从理论上说,202g茉莉醛能从足量银氨溶液中还原出216g银 |
几种物质的熔点如下表:
据此作出的下列判断中错误的是( )
| 物质 | Na2O | NaCl | AlF3 | AlCl3 | BCl3 | Al2O3 | CO2 | SiO2 |
| 熔点/℃ | 920 | 801 | 1291 | 190 | -107 | 2073 | -57 | 1723 |
| A、铝的化合物的晶体中,有的是离子晶体 |
| B、表中物质里只有BCl3和CO2的晶体是分子晶体 |
| C、同主族元素的氧化物可能形成不同类型的晶体 |
| D、不同主族元素的氧化物可能形成相同类型的晶体 |
下列关于碱金属的说法中,正确的是( )
| A、碱金属单质的密度都比水轻,投入水中都能浮在水面上 |
| B、碱金属单质都是还原剂,其还原性随着核电荷数的增大而增强 |
| C、碱金属单质的熔沸点一般随着原子的电子层数的增多而升高 |
| D、碱金属单质在氧气中燃烧,产物都是过氧化物 |

 某研究性学习小组对还原铁粉与水蒸气的反应及产物进行科学探究.
某研究性学习小组对还原铁粉与水蒸气的反应及产物进行科学探究. 小苏打作为食品制作过程中的膨松剂在食品加工产业上有广泛的用途.
小苏打作为食品制作过程中的膨松剂在食品加工产业上有广泛的用途.