题目内容
14.下列反应的离子方程式正确的是( )| A. | 过量CO2通入NaOH溶液中:CO2+2OH-═CO32-+H2O | |
| B. | 铜与足量浓硝酸反应:Cu+4H++2NO3-═Cu2++2NO↑+2H2O | |
| C. | 碳酸钠固体溶于水:CO32-+2H2O?H2CO3+2OH- | |
| D. | 钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ |
分析 A.二氧化碳过量,反应生成碳酸氢根离子;
B.铜与浓硝酸反应生成的是二氧化氮;
C.碳酸根离子的水解分步进行,主要以第一步为主;
D.钠与水反应生成氢氧化钠和氢气.
解答 解:A.过量CO2通入NaOH溶液中,反应生成碳酸氢钠,正确的离子方程式为:CO2+OH-═HCO3-,
B.铜与足量浓硝酸反应生成硝酸铜、二氧化氮和水,正确的离子方程式为:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O,故B错误;
C.碳酸钠固体溶于水电离出碳酸根离子和钠离子,碳酸根离子的水解方程式需要分步书写,主要以第一步为主,正确的离子方程式为:CO32-+H2O?HCO3-+OH-,故C错误;
D.Na与水反应生成氢氧化钠和氢气,反应的离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,故D正确;
故选D.
点评 本题考查了离子方程式的判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等

练习册系列答案
相关题目
4.下列物质中,既能和盐酸反应,又能和氢氧化钠反应的化合物是( )
| A. | 碳酸钠 | B. | 碳酸氢钠 | C. | 铝箔 | D. | 磁性氧化铁 |
5.关于氧气(O2)和臭氧(O3)说法正确的是( )
| A. | 互为同素异形体 | |
| B. | 二者相互转化是物理变化 | |
| C. | 同温同压下,等体积的氧气和臭氧含有相同的分子数 | |
| D. | 等物质的量的氧气和臭氧含有相同的质子数 |
9.下列叙述正确的是( )
(1)c(H+)═c(OH-)=10-6mol/L的溶液一定呈中性
(2)已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3kJ•mol-1,则含40.0g NaOH的稀溶液与稀醋酸完全中和,放出57.3kJ的热量
(3)向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2悬浊液,加热,无砖红色沉淀生成,说明淀粉没有水解生成葡萄糖
(4)同一主族的元素,原子半径越大,其单质的熔点不一定越高
(5)乙酸乙酯在NaOH溶液(H218O)中水解产物为CH3CO18ONa和CH3CH2OH
(6)水的电子式 H+[:O:]2-H+.
(1)c(H+)═c(OH-)=10-6mol/L的溶液一定呈中性
(2)已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3kJ•mol-1,则含40.0g NaOH的稀溶液与稀醋酸完全中和,放出57.3kJ的热量
(3)向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2悬浊液,加热,无砖红色沉淀生成,说明淀粉没有水解生成葡萄糖
(4)同一主族的元素,原子半径越大,其单质的熔点不一定越高
(5)乙酸乙酯在NaOH溶液(H218O)中水解产物为CH3CO18ONa和CH3CH2OH
(6)水的电子式 H+[:O:]2-H+.
| A. | (1)(2)(5)(6) | B. | (1)(4)(5) | C. | (2)(4)(6) | D. | 全部 |
6.下列关于各图的叙述,正确的是( )
| A. | 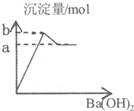 图表示向明矾溶液中滴加Ba(OH)2溶液产生沉淀的量关系曲线 | |
| B. | 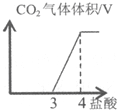 图表示向含有等物质的量的NaOH和Na2CO3溶液中加入盐酸放出CO2的关系曲线 | |
| C. | 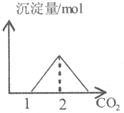 图表示向含有等物质的量的NaOH和Ca(OH)2溶液中通入CO2的产生沉淀关系曲线 | |
| D. |  图表示向NaOH溶液中滴加AlCl3溶液产生沉淀的量关系曲线 |
3.下列化学用语表示正确的是( )
| A. | 葡萄糖的最简式(实验式):CH2O | B. | 乙烯的结构简式为:CH2CH2 | ||
| C. | 氮气的电子式: | D. | 核内有8个中子的碳原子:86C |
 化学是一门以实验为基础的学科.
化学是一门以实验为基础的学科. 一定温度下,在2L的恒容密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
一定温度下,在2L的恒容密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示: