题目内容
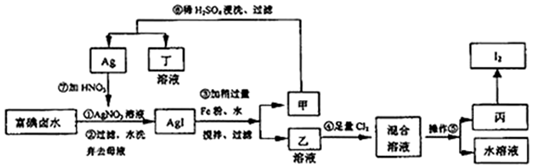
12.某种盐溶解后得到的溶液中,可能含有Fe2+、Fe3+、SO42-、NH4+、Ba2+、CO32-离子中的某几种.(1)甲同学做如下实验:①取少量溶液于试管中,逐滴加入浓氢氧化钠溶液,发现先生成白色沉淀,迅速变为灰绿色,最后变为红褐色,并有刺激性气体生成;②另取少量溶液于试管中,加入少量盐酸酸化的氯化钡溶液,有白色沉淀生成.该溶液中一定含有的离子是Fe2+、SO42-、NH4+;
(2)乙同学做如下实验:取少量溶液于试管中,滴加几滴硫氰化钾溶液,无明显现象;再滴加H2O2,发现溶液变红色;继续滴加H2O2,红色逐渐褪去且有气泡产生.为弄清其中缘由,他查阅资料知:
H2O2+SCN-→SO42-+CO2↑+N2↑+H2O+H+(SCN-中S为-2价)
①该反应中,被氧化的元素为N、S,每生成lmol CO2转移的电子数为11 NA;
②根据乙同学的实验现象,请判断还原性强弱为:Fe2+>SCN-(填<、=或>);
(3)金属表面处理、皮革鞣制、印染等都可能造成铬污染.六价铬比三价铬毒性强更易被人体吸收且在体内蓄积.工业上处理酸性含Cr2O72-废水的方法如下:
①向含Cr2O72-的酸性废水中加入FeSO4溶液,使Cr2O72-全部转化为Cr3+.写出该反应的离子方程式:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O.
②铬元素总浓度的测定:准确移取25.00mL含Cr2O72-和Cr3+的酸性废水,向其中加入足量的(NH4)2S2O8溶液将Cr3+氧化成Cr2O72-,煮沸除去过量的(NH4)2S2O8;向上述溶液中加入过量的KI溶液,充分反应后以淀粉为指示剂,向其中滴加0.015mol•L-1的Na2S2O3标准溶液,终点时消耗Na2S2O3溶液20.00ml.计算废水中铬元素总浓度208mg•L-l (已知I2+2S2O32-=2I-+S4O62-)
分析 (1)①取少量溶液于试管中,逐滴加入浓氢氧化钠溶液,发现开始生成白色沉淀,则不含Fe3+,白色沉淀迅速变为灰绿色,最后变为红褐色,说明含有Fe2+,则一定不含CO32-,同时伴有刺激性气体放出,应为氨气,说明含有Fe2+;
②另取少量溶液于试管中,加入足量盐酸酸化后再滴加氯化钡溶液,有白色沉淀生成,说明含有SO42-,则不含Ba2+;
(2)乙同学进行如下实验:取少量溶液于试管中,滴加几滴硫氰酸钾溶液,无明显现象;再滴加H2O2,发现溶液变红色,说明含有Fe2+,不含Fe3+;继续滴加H2O2,红色逐渐褪去且有气泡产生,发生H2O2+SCN-→SO42-+CO2↑+N2↑+H2O+H+,反应中N、S盐酸化合价升高,被氧化,结合化合价的变化以及物质的性质解答该题;
(3)①Cr2O72-的酸性工业废水中加入硫酸亚铁反应生成铁离子,三价铬离子和水,依据原子守恒和电荷守恒配平书写离子方程式;
②根据铬原子守恒,计算总Cr2O72-的物质的量,再根据废水中铬元素总浓度=$\frac{m(Cr)}{V}$进行计算,结合关系式Cr2O72-~6I-~6S2O32-计算.
解答 解:(1)取少量溶液于试管中,逐滴加入浓氢氧化钠溶液,发现开始生成白色沉淀,则不含Fe3+,白色沉淀迅速变为灰绿色,最后变为红褐色,说明含有Fe2+,发生反应为4Fe(OH)2+O2+2H2O=4Fe(OH)3,则一定不含CO32-,同时伴有刺激性气体放出,应为氨气,说明含有Fe2+;
②另取少量溶液于试管中,加入足量盐酸酸化后再滴加氯化钡溶液,有白色沉淀生成,说明含有SO42-,则不含Ba2+,所以一定含有的离子是Fe2+、SO42-、NH4+,
故答案为:Fe2+、SO42-、NH4+;
(2)①乙同学进行如下实验:取少量溶液于试管中,滴加几滴硫氰酸钾溶液,无明显现象;再滴加H2O2,发现溶液变红色,说明含有Fe2+,不含Fe3+;继续滴加H2O2,红色逐渐褪去且有气泡产生,发生H2O2+SCN-→SO42-+CO2↑+N2↑+H2O+H+,反应中N、S盐酸化合价升高,S元素化合价有-2价升高到+6价,N元素化合价由-3价升高到0价,被氧化,每生成lmol CO2,有方程式可知生成1molSO42-,0.5mol+N2,转移的电子的物质的量为1mol×8+0.5mol×2×3=11mol,为11NA个,
故答案为:N、S;11;
②由反应的先后顺序可知过氧化氢先氧化Fe2+,则Fe2+还原性较强,
故答案为:>;
(3)①工业上为了处理含有Cr2O72-的酸性工业废水,用FeSO4溶液把废水中的六价铬离子还原成三价铬离子,Cr2O72-的酸性工业废水中加入硫酸亚铁反应生成铁离子,三价铬离子和水,反应的离子方程式为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O,
故答案为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O;
②由①2Cr3++3S2O82-+7H2O═Cr2O72-+6SO42-+14H+
②Cr2O72-+6I-+14H+═2Cr3++3I2+7H2O
③I2+2S2O32-═2I-+S4O62-.
则Cr2O72-~6I-~6S2O32-
1 6
n 0.015×20×10-3
n=$\frac{0.015×20×1{0}^{-3}}{6}$=0.05×10-3,则根据铬原子守恒,25.00mL含Cr2O72-和Cr3+的酸性废水铬元素总浓度=$\frac{0.05×1{0}^{-3}×2×52×1{0}^{3}mg}{25×1{0}^{-3}L}$=208mg•L-1,故答案为:208.
点评 本题考查了常见离子的性质及检验方法,为高频考点,题目难度中等,注意掌握离子反应发生条件,明确常见离子的检验方法,试题培养了学生的分析、理解能力及逻辑推理能力.

| A. | 点燃氢气前一定要检验氢气的纯度 | |
| B. | 未使用完的白磷要随时收集起来,并与空气隔绝 | |
| C. | 酒精灯不用时,必须盖上灯帽 | |
| D. | 用CO还原氧化铁时,要先通一会儿CO气体,再加热氧化铁 |
| A. | 油脂可用于制造肥皂 | |
| B. | 小苏打可用于治疗胃酸过多 | |
| C. | 氢氧化铁胶体用于消毒净水 | |
| D. | 热的碳酸钠溶液可去除铜片表面的油污 |
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| (1) | 2 | 3 | 0 | 27.78kJ |
| (2) | 1.6 | 1.8 | 0.8 | Q |
| A. | 容器(2)中反应开始时v(正)>v(逆) | |
| B. | 容器(1)、(2)中反应达平衡时压强相等 | |
| C. | 容器(2)中反应达平衡时,吸收的热量Q为9.26 kJ | |
| D. | 若条件为“绝热恒容”,容器(1)中反应达平衡时n (NH3)<0.6 mol |
| A. | 0.40mol | B. | 0.50mol | C. | 0.60mol | D. | 0.70mol |
| 编号 | 温度(℃) | 起始/mol | 平衡/mol | 达到平衡 所需时间/s | |
| PCl5(g) | PCl3(g) | Cl2(g) | |||
| Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t1 |
| Ⅱ | 320 | 0.80 | t2 | ||
| Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t3 |
| A. | 平衡常数K:容器Ⅱ>容器Ⅲ | |
| B. | 反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ | |
| C. | 反应到达平衡时,容器I中的平均速率为v(PCl5)=0.1/t1 mol•L-1•s-1 | |
| D. | 容器Ⅲ中平衡后,等温条件下充入一定量He,平衡不发生移动 |
 ;
; .
.