题目内容
14. 工业上制取氯酸钾的主要步骤为:
工业上制取氯酸钾的主要步骤为:I.将C12 通入石灰浆,充分反应后过滤;
II.向滤液中加入稍过量的KCl固体,进行适当操作可析出KCIO3固体.
请回答下列问题:
步骤I存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,总反应的化学方程式为
6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6H2O.
(1)①标出反应6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6H2O 中电子转移的方向和数目
②滤液中Ca(ClO3)2与CaC12的物质的量之比n[Ca(ClO)2]:n[CaCl2]<l:5 (填“>”、“<”或“=”),理由是同时还发生反应2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.(请用有关反应和必要的文字进行说明)
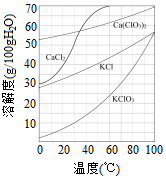
(2)如图是有关物质的溶解度曲线.步骤II中,若溶液中KCIO3的含量为100g•L-1,从该溶液中尽可能多地析出KClO3 固体的方法是蒸发浓缩、冷却结晶.
分析 (1)①根据化合价升降判断氧化剂和还原剂,结合化学计量数得出得失电子总数,反应6Cl2+6Ca(OH)2=5CaCl2+Ca(ClO3)2+6H2O中只有Cl元素化合价发生变化,由0价分别变化为+5价、-1价;
②部分氯气与冷的氢氧化钙反应生成氯化钙、次氯酸钙和水;
(2)经蒸发浓缩、冷却结晶可得晶体KClO3.
解答 解:(1)①反应6Cl2+6Ca(OH)2=5CaCl2+Ca(ClO3)2+6H2O中只有Cl元素化合价发生变化,由0价分别变化为+5价、-1价,氯气既是氧化剂也是还原剂,由方程式可知反应6mol氯气时生成1molCa(ClO3)2,转移10mol电子,则表示子转移的方向和数目为: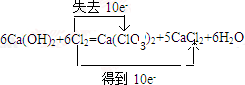 ;故答案为:
;故答案为: ;
;
②部分氯气与冷的氢氧化钙反应2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,也生成氯化钙,所以n(Ca(ClO3)2):n(CaCl2)<l:5,
故答案为:<;同时还发生反应2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
(2)该溶液中尽可能多地析出KClO3固体,应经蒸发浓缩、冷却结晶,
故答案为:蒸发浓缩、冷却结晶.
点评 本题考查物质的制备,为高考常见题型和高频考点,侧重于学生的分析能力的考查,解答本题注意把握物质的性质以及题给信息,题目难度中等.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
5.下列化学用语表示正确的是( )
| A. | 正丁烷的结构简式:C4H10 | |
| B. | S2-的结构示意图: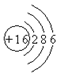 | |
| C. | NH3的电子式: | |
| D. | 碳酸钠电离方程式:Na2CO3=Na++CO32- |
2.配制一定体积、一定物质的量浓度的溶液,下列操作会使配得的溶液浓度偏小的是( )
| A. | 容量瓶中原有少量蒸馏水 | |
| B. | 溶液从烧杯转移到容量瓶后没有洗涤烧杯 | |
| C. | 未冷却即将溶液转移到容量瓶 | |
| D. | 加水未达到容量瓶刻度线 |
9.分类法在化学科学中起着非常重要的作用,下列各组物质中,在物质分类型,前者从属于后者的一组是( )
| A. | 金属,化合物 | B. | 金属氧化物,碱性氧化物 | ||
| C. | 泥沙,胶体 | D. | 单质,纯净物 |
6.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 2.4g镁在足量的氧气中燃烧,转移的电子数为0.1NA | |
| B. | 标准状况下,5.6L二氧化碳气体中含有的氧原子数为0.5NA | |
| C. | 氯原子数为0.2NA的氯气溶于水转移的电子数0.1NA | |
| D. | 0.1L0.5mol/LCH3COOH溶液中含有的氢离子数为0.05NA |