题目内容
20.选择下列物质,填写以下空白.(请填字母)A.干冰B.氧化镁C.甲烷D.纯碱E.固体氖F.氟化钾G.金刚石H.氯化钾I.硫化铵
(1)熔化时,不需要破坏化学键的是ACE.
(2)熔点最高的是,由原子直接构成的是H.
(3)晶体中既有离子键,又有共价键的是DI,试比较不含共价键的离子晶体的熔沸点,由高到低的排序为B>F>H.
(4)二氧化碳分子构型为直线型,12g甲烷中含有molC-H键.
分析 A.干冰是分子晶体,熔化时,破坏分子间作用力;
B.氧化镁是离子晶体,熔化时破坏离子键;
C.甲烷是分子晶体,熔化时,破坏分子间作用力;
D.纯碱是离子晶体,熔化时破坏离子键;
E.固体氖是单原子分子,熔化时,破坏分子间作用力;
F.氟化钾是离子晶体,熔化时破坏离子键;
G.金刚石是原子晶体,熔化时破坏共价键;
H.氯化钾是离子晶体,熔化时破坏离子键;
I.硫化铵是离子晶体,熔化时破坏离子键.
解答 解:(1)分子晶体熔化时,破坏分子间作用力,所以不需要破坏化学键的是ACE;
故答案为:ACE;
(2)一般来说,原子晶体的熔点高于离子晶体,离子晶体的熔点高于分子晶体,所以熔点最高,由原子直接构成的是金刚石;
故答案为:H;
(3)纯碱中含有离子键和共价键,硫化铵中含有离子键和共价键,所以晶体中既有离子键,又有共价键的是DI;离子晶体中离子半径越小,离子所带电荷越多,离子晶体的熔沸点越高,所以熔沸点:氧化镁>氟化钾>氯化钾,即B>F>H;
故答案为:DI;B>F>H;
(4)二氧化碳分子构型为直线型分子,12g甲烷即1mol,含有4molC-H键;
故答案为:直线;4.
点评 本题考查晶体类型的判断、晶体中粒子间作用力、分子的空间构型等知识点,题目难度不大,注意知识的积累,侧重于考查学生对基础知识的应用能力.

练习册系列答案
相关题目
11.通常人们把拆开1mol某化学键所吸收的能量或形成1mol某化学键所释放的能量看成该化学键的键能.已知热化学方程式:N2(g)+3H2(g)=2NH3(g)△H=-92.4kJ/mol,请根据热化学方程式和表中数据计算:H-N键的键能x约为( )
| 化学键 | H-H | N≡N | H-N |
| 键能 | 436kJ/mol | 946kJ/mol | x |
| A. | 391kJ/mol | B. | 431kJ/mol | C. | 349kJ/mol | D. | 469kJ/mol |
8.下列指定反应的离子方程式正确的是( )
| A. | 将铜插入稀硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| B. | 向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe═2Fe2+ | |
| C. | 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3﹒H2O═Al(OH)3↓+3NH4+ | |
| D. | 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+═H2SiO3↓+2Na+ |
15.如括号内为杂质,以下所用的除杂方法正确的是( )
①氯气(HCl):气体通过饱和食盐水
②NaCl固体(I2):升华
③NaBr溶液(NaCl):加AgNO3溶液过滤
④溴水(I2):加苯萃取后分液.
①氯气(HCl):气体通过饱和食盐水
②NaCl固体(I2):升华
③NaBr溶液(NaCl):加AgNO3溶液过滤
④溴水(I2):加苯萃取后分液.
| A. | ①② | B. | ③④ | C. | ①②③ | D. | 全部 |
5.下列关于NH4HS溶液的叙述正确的是( )
| A. | 该溶液中,K+、Cu2+、Cl-、ClO-可以大量共存 | |
| B. | 和FeCl3溶液反应的离子方程式:HS-+2Fe3+═S↓+2Fe2++H+ | |
| C. | 和过量NaOH溶液反应的离子方程式:HS-+OH-═S2-+H2O | |
| D. | 向该溶液中通入过量的SO2,无沉淀生成 |
12.下列离子反应中,表达正确的是( )
| A. | 过量的SO2通入NaOH溶液中:SO2+2OH-═SO32-+H2O | |
| B. | 用醋酸溶解CaCO3:2H+CaCO3═Ca2++H2O+CO2↑ | |
| C. | 在氯化亚铁溶液中通入氯气Fe2++Cl2═Fe3++2Cl- | |
| D. | NaHCO3溶液中加入过量的Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O |
9.如图所示的五种尾气吸收装置中,适合吸收极易溶于水的气体,且能防止产生倒吸现象(溶液进入气体发生装置中)的是( )
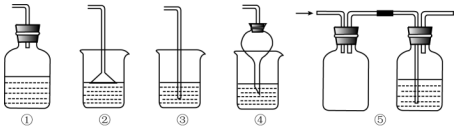

| A. | ②④⑤ | B. | ①②④ | C. | ①②③ | D. | ①②④⑤ |