题目内容
14.有关如图所示原电池的叙述正确的是( )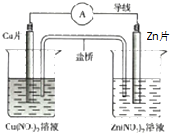
| A. | 盐桥中阴离子向正极移动 | |
| B. | 正极的电极反应是:Zn2++2e-═Zn | |
| C. | Zn片上发生氧化反应 | |
| D. | 用该电池电解水,析出3.2gCu时生成1.12LO2(标况下) |
分析 图为原电池装置,Zn为负极,发生氧化反应Zn-2e-═Zn2+,Cu为正极,发生还原反应Cu2++2e-═Cu,原电池工作时,阳离子向正极移动,阴离子向负极移动,结合电子守恒解答该题.
解答 解:A.盐桥中阴离子向负极移动,故A错误;
B.Cu为正极,溶液中的铜离子在正极上发生还原反应,正极的电极反应是:Cu2++2e-═Cu,故B错误;
C.Zn为负极,失电子发生氧化反应,故C正确,
D.3.2gCu的物质的量为0.05mol,转移电子为0.1mol,根据电子守恒可知,电解水生成氧气为0.1mol×$\frac{1}{4}$=0.025mol,在标准状况下体积为0.56L,故D错误;
故选:C.
点评 本题考查原电池的工作原理,题目难度不大,注意电极的判断和电极方程式的书写,注意把握原电池的工作原理和电子守恒在计算中的应用,学习中注意相关知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.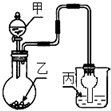 用如图装置进行实验,甲逐滴加入到固体乙中,如表说法正确的是( )
用如图装置进行实验,甲逐滴加入到固体乙中,如表说法正确的是( )
 用如图装置进行实验,甲逐滴加入到固体乙中,如表说法正确的是( )
用如图装置进行实验,甲逐滴加入到固体乙中,如表说法正确的是( )| 选项 | 液体甲 | 固体乙 | 溶液丙 | 丙中现象 |
| A | CH3COOH | NaHCO3 | 苯酚钠 | 无明显现象 |
| B | 浓HCl | KMnO4 | 紫色石蕊 | 最终呈红色 |
| C | 浓H2SO4 | Na2SO3 | 品红 | 红色变无色 |
| D | 浓H2SO4 | Cu | 氢硫酸 | 溶液变浑浊 |
| A. | A | B. | B | C. | C | D. | D |
9.Ⅰ.现有浓度均为0.1mol•L -1的下列溶液:
①硫酸 ②醋酸 ③氢氧化钠 ④氯化铵 ⑤醋酸铵 ⑥硫酸铵 ⑦硫酸氢铵 ⑧氨
水,请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)④②③①.
(2)④、⑤、⑥、⑦、⑧五种溶液中NH4+浓度由大到小的顺序是(填序号)⑥⑦④⑤⑧.
(3)将③和④等体积混合后,混合液中各离子浓度关系正确的是A.
A.c(Na+)=c(C1-)>c(OH-)>c(NH4+)
B.c(Na+)=0.1mol•L-1
C.c(Na+)+c(NH4+)=c(C1-)+c(OH-)
D.c(H+)>c(OH-)
Ⅱ.如表是不同温度下水的离子积的数据:
试回答以下问题:
(1)若25<t l<t 2,则a>1×10-14(填“>”、“<”或“=”),做此判断的理由是水的电离为吸热反应,升高温度,平衡向着正反应方向移动.
(2)25℃时,某Na2S04溶液中c(S042-)=5×10-4 mol•L-1,取该溶液l mL加水稀释至10mL,则
稀释后溶液中c(Na+):c(OH-)=1000:1.
(3)在t2温度下,将pH=11的NaOH溶液a L与pH=1的H2S04溶液b L混合,若所得混合液pH=2,则a:b=9:11.
①硫酸 ②醋酸 ③氢氧化钠 ④氯化铵 ⑤醋酸铵 ⑥硫酸铵 ⑦硫酸氢铵 ⑧氨
水,请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)④②③①.
(2)④、⑤、⑥、⑦、⑧五种溶液中NH4+浓度由大到小的顺序是(填序号)⑥⑦④⑤⑧.
(3)将③和④等体积混合后,混合液中各离子浓度关系正确的是A.
A.c(Na+)=c(C1-)>c(OH-)>c(NH4+)
B.c(Na+)=0.1mol•L-1
C.c(Na+)+c(NH4+)=c(C1-)+c(OH-)
D.c(H+)>c(OH-)
Ⅱ.如表是不同温度下水的离子积的数据:
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积 | 1×10-14 | a | 1×10-12 |
(1)若25<t l<t 2,则a>1×10-14(填“>”、“<”或“=”),做此判断的理由是水的电离为吸热反应,升高温度,平衡向着正反应方向移动.
(2)25℃时,某Na2S04溶液中c(S042-)=5×10-4 mol•L-1,取该溶液l mL加水稀释至10mL,则
稀释后溶液中c(Na+):c(OH-)=1000:1.
(3)在t2温度下,将pH=11的NaOH溶液a L与pH=1的H2S04溶液b L混合,若所得混合液pH=2,则a:b=9:11.
3.在一定温度下,a的容积保持不变,b的上盖可随容器内气体压强的改变而上下移动,以保持容器内外压强相等.在a、b中分别加入2mol A和2molB,起始时容器体积均为V L,发生反应2A+B?xC,并达到化学平衡状态,平衡时两容器中A、B、C的物质的量之比均为1:3:6.下列说法一定正确的是( )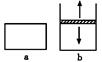

| A. | x的值为2 | |
| B. | B物质可为固体或液体 | |
| C. | 平衡时,a容器的体积小于V L | |
| D. | a、b容器中从起始到平衡所需时间相同 |
 ,其与过量的NaOH溶液反应的化学方程式是
,其与过量的NaOH溶液反应的化学方程式是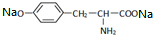 +2H2O.
+2H2O.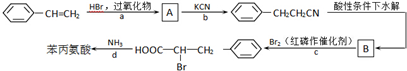
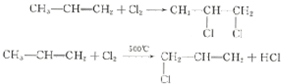
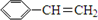 +HBr→
+HBr→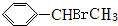 .
. +Br2$\stackrel{红磷}{→}$
+Br2$\stackrel{红磷}{→}$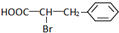 +HBr.
+HBr.
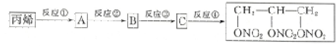
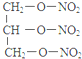 +3H2O.
+3H2O.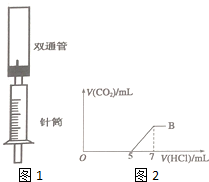 为探究Na2CO3与盐酸的反应原理,设计了如图1实验装置.
为探究Na2CO3与盐酸的反应原理,设计了如图1实验装置.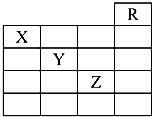 如图是元素周期表的一部分,关于元素X、Y、Z的叙述中,正确的个数是( )
如图是元素周期表的一部分,关于元素X、Y、Z的叙述中,正确的个数是( )