题目内容
2.下列反应在一定条件下可以实现的是( )①酸性氧化物与碱反应
②有单质参加的非氧化还原反应
③没有水生成,也没有沉淀和气体生成的复分解反应
④两种酸溶液充分反应后的溶液呈中性.
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
分析 ①酸性氧化物是和碱反应生成水和盐的氧化物;
②有元素化合价变化的反应属于氧化还原反应;
③没有水生成,也没有沉淀和气体生成的复分解反应,发生络合反应符合这一要求;
④氧化还原反应的发生有可能使得溶液的酸碱性发生变化.
解答 解:①酸性氧化物是和碱反应生成水和盐的氧化物,如二氧化碳可以和氢氧化钠发生反应生成碳酸钠和水,故正确;
②同素异形体之间的转化属于有单质参加的非氧化和还原反应,故正确;
③没有水生成,也没有沉淀和气体生成的复分解反应,如 Fe3++3SCN-?Fe(SCN)3)硫氰化铁为血红色物质,既不是沉淀也不是气体,故正确;
④根据反应2H2S+H2SO3=3H2O+S↓可以知道:氢硫酸和亚硫酸溶液充分反应后的溶液体系为中性,故正确;
故选D.
点评 本题考查学生元素和化合物的综合知识,注意知识的积累是解题的关键,综合性较强,难度较大.

练习册系列答案
相关题目
12.下列离子方程式中,不正确的是( )
| A. | 向FeBr2溶液中通入少量的Cl2:2Fe2++Cl2═2Fe3++2Cl- | |
| B. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2恰好使SO42-反应完全:2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O | |
| C. | 向Ca(HCO3)2溶液中加入过量的NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| D. | 向Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
13.下列有关氮元素及其化合物的表示正确的是( )
| A. | 质子数为7、中子数为8的氮原子:${\;}_{7}^{8}$N | |
| B. | 溴化铵的电子式: | |
| C. | 氮原子的结构示意图: | |
| D. | 间硝基甲苯的结构简式: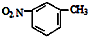 |
10.下列关于“化学与健康”的说法不正确的是( )
| A. | 服用铬含量超标的药用胶囊会对人对健康造成危害 | |
| B. | 食用一定量的油脂能促进人体对某些维生素的吸收 | |
| C. | “血液透析”利用了胶体的性质 | |
| D. | 使用填埋法处理未经分类的生活垃圾 |
7.硝酸与金属反应往往产生氮氧化物,但是在某些特殊情况则不然.将稀硝酸(HNO3浓度低于2mol•L-1)与过量金属镁缓和反应放出气体A,反应完全后向剩余溶液中加入过量NaOH固体并加热,放出气体B,将两次放出气体全部收集并混合,用碱石灰干燥后缓慢通过足量的灼热氧化铜固体,观察到固体变红,将剩余气体用浓硫酸干燥,气体体积变为原来的三分之一,则下列分析不正确的是(本题中所有气体体积均为相同条件下测得的体积)( )
| A. | 灼热氧化铜变红过程发生的反应有2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$N2+3H2O+3Cu | |
| B. | 气体A为H2;气体B为NH3 | |
| C. | 气体A与气体B的体积比为1:2 | |
| D. | 在镁与硝酸反应过程中还原剂与氧化剂的物质的量之比为3:2 |
12.下列离子方程式的书写正确的是( )
| A. | 铁和稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | NaHCO3溶液与NaOH溶液反应:OH-+HCO3-═CO32-+H2O | |
| C. | 钠和冷水反应:Na+2H2O═Na++2OH-+H2↑ | |
| D. | 氯化铝溶液中加入过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
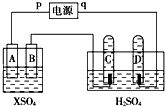 如图,p、q为直流电源的两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D极上均产生气泡,试回答:
如图,p、q为直流电源的两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D极上均产生气泡,试回答: