题目内容
如果1gCO2中含有m个氧原子,则阿伏加德罗常数的数值是( )
| A、1/22m | B、22m |
| C、12m | D、44m |
考点:物质的量的相关计算
专题:计算题
分析:根据n=
计算二氧化碳的物质的量,氧原子物质的量为二氧化碳的2倍,再根据N=nNA计算.
| m |
| M |
解答:
解:1gCO2 的物质的量=
=
mol,氧原子物质的量为二氧化碳的2倍,故
mol×2×NAmol-1=m,故NA=22m,故选B.
| 1g |
| 44g/mol |
| 1 |
| 44 |
| 1 |
| 44 |
点评:本题考查阿伏伽德罗常数,比较基础,注意对公式的理解与灵活应用.

练习册系列答案
相关题目
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
| B、常温常压下,16gO2和O3的混合气体中含有的原子总数为NA |
| C、标准状况下,11.2LH2O中含有分子的数目为0.5NA |
| D、2.4g金属镁变成镁离子时失去的电子数目为0.1NA |
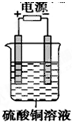 如图所示,用惰性电极电解硫酸铜溶液,下列有关叙述正确的是( )
如图所示,用惰性电极电解硫酸铜溶液,下列有关叙述正确的是( )| A、阴极上的电极反应为:2H++2e-=H2 |
| B、电解一段时间后,溶液的酸碱性不变 |
| C、电解一段时间后,阴极的质量增加,阳极上有大量气泡产生 |
| D、若将石墨电极都换成铁电极,电解一段时间后,两电极质量不变 |
 随着日本福岛核电站放射性碘泄漏,碘这种元素被人们所认知.如图是元素周期表中提供的碘元素的部分信息及碘原子的结构示意图.下列说法错误的是( )
随着日本福岛核电站放射性碘泄漏,碘这种元素被人们所认知.如图是元素周期表中提供的碘元素的部分信息及碘原子的结构示意图.下列说法错误的是( )| A、碘的相对原子质量为126.9,原子核内质子数为53 |
| B、碘原子核外共有53个电子,最外层有7个电子 |
| C、碘元素属于非金属元素,碘原子在化学反应中容易得到电子 |
| D、碘盐中含有碘酸钾(KIO3),KIO3中碘元素的化合价为-1价 |
下列说法正确的是( )
| A、用湿润的PH试纸可测溶液的酸碱性 |
| B、用碱式滴定管可量取5.00mLKMnO4溶液 |
| C、碳酸钠溶液可盛放于玻璃瓶塞的试剂瓶内 |
| D、氯水可用棕色试剂瓶保存于阴暗处 |
相同温度、相同物质的量浓度的下列溶液:①Na2SO4、②NaHSO4、③NH4HSO4,按pH值由小到大的顺序排列,应是( )
| A、③<②<① |
| B、②<①<③ |
| C、②<③<① |
| D、①<②<③ |
有机物与足量的钠混合熔融时,其中的元素可转化为含钠的化合物.下列有关有机物与足量钠反应,各元素的转化结果正确的是( )
| A、碳元素转化在氰化钠中 |
| B、氯元素转化在高氯酸钠中 |
| C、溴元素转化在溴化钠中 |
| D、硫元素转化在硫酸钠中 |
已知G、Q、X、Y、Z均为含氯元素的化合物,在一定条件下有下列转化关系(未配平):
①G→Q+NaCl
②Q+H2O
X+H2
③Y+NaOH-→G+Q+H2O
④Z+NaOH-→Q+X+H2O
这五种化合物中Cl元素化合价由低到高的顺序是( )
①G→Q+NaCl
②Q+H2O
| ||
③Y+NaOH-→G+Q+H2O
④Z+NaOH-→Q+X+H2O
这五种化合物中Cl元素化合价由低到高的顺序是( )
| A、G、Y、Q、Z、X |
| B、X、Z、Q、G、Y |
| C、X、Z、Q、Y、G |
| D、G、Q、Y、Z、X |