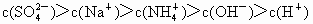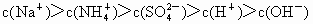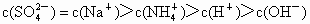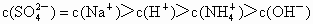题目内容
把浓度均为0.1mol?L-1的NaOH溶液、H2SO4溶液和氨水等体积混合,所得混合液中各种离子浓度的大小顺序是( )
| A、c(SO42-)>c(Na+)>c(NH4+)>c(OH-)>c(H+) | B、c(Na+)>c(NH4+)>c(SO42-)>c(H+)>c(OH-) | C、c(SO42-)=c(Na+)>c(NH4+)>c(H+)>c(OH-) | D、c(SO42-)=c(Na+)>c(H+)>c(NH4+)>c(OH-) |
分析:把浓度均为0.1mol?L-1的NaOH溶液、H2SO4溶液和氨水等体积混合,依据化学方程式分析得到溶液中溶质为同浓度的Na2SO4、(NH4)2SO4的溶液,溶液中铵根离子水解显酸性,硫酸根离子浓度等于钠离子浓度.
解答:解:由化学反应方程式及量的关系,2NaOH+H2SO4=Na2SO4+2H2O 2NH3?H2O+H2SO4=(NH4)2SO4+2H2O,最后得到的是同浓度的Na2SO4、(NH4)2SO4的溶液,由于NH4+水解显酸性,使得c(H+)>c(OH-),得到溶液中离子浓度大小为:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-),
答案:C
答案:C
点评:本题考查了化学反应和溶液中产物判断,溶液中盐类水解的分析应用,掌握基础是关键,题目难度中等.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
把浓度均为0.1mol/L的NaOH溶液、H2SO4溶液和氨水等体积混合,所得混合液中各种离子浓度的大小顺序正确的是
A.[SO42-]>[Na+]>[NH4+]>[OH-] >[H+] >[H+] | B.[Na+]>[NH4+]>[SO42-]>[H+]>[OH-] |
| C.[SO42-]=[Na+]>[NH4+]>[H+]>[OH-] | D.[SO42-]=[Na+]>[H+]>[NH4+]>[OH-] |
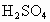 溶液和氨水等体积混合,所得混合液中各种离子浓度的大小顺序是
溶液和氨水等体积混合,所得混合液中各种离子浓度的大小顺序是