题目内容
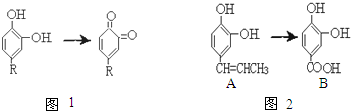
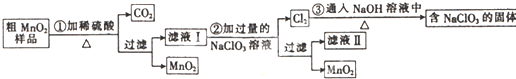
 通过资源化利用的方式将CO2转化为具有工业应用价值的产品(如图所示),是一种较为理想的减排方式,下列说法中正确的是( )
通过资源化利用的方式将CO2转化为具有工业应用价值的产品(如图所示),是一种较为理想的减排方式,下列说法中正确的是( )| A、CO2经催化分解为C、CO、O2的反应为放热反应 |
| B、除去Na2CO3固体中少量NaHCO3可用热分解的方法 |
| C、过氧化尿素和SO2都能使品红溶液褪色,其原理相同 |
| D、由CO2和H2合成甲醇,原子利用率达100% |
考点:物质的分离、提纯的基本方法选择与应用,绿色化学,物质分离和提纯的方法和基本操作综合应用
专题:
分析:A.根据能量守恒分析;
B.碳酸氢钠不稳定,加热时易分解生成碳酸钠;
C.过氧化尿素具有强氧化性,二氧化硫能和有色物质反应生成无色物质;
D.化学反应中除了目标产物外没有其它物质生成时,原子利用率为100%.
B.碳酸氢钠不稳定,加热时易分解生成碳酸钠;
C.过氧化尿素具有强氧化性,二氧化硫能和有色物质反应生成无色物质;
D.化学反应中除了目标产物外没有其它物质生成时,原子利用率为100%.
解答:
解:A.二氧化碳高温分解需要吸收能量,根据能量守恒知,该反应是吸热反应,故A错误;
B.碳酸氢钠不稳定,加热时易分解生成碳酸钠,碳酸钠较稳定,加热时不易分解,所以除去碳酸钠固体中少量NaHCO3可用热分解的方法,故B正确;
C.过氧化尿素的漂白性是利用其强氧化性,二氧化硫的漂白性是利用其和有色物质反应生成无色物质,所以反应原理不同,故C错误;
D.二氧化碳合成甲醇时,除了生成甲醇外还生成其它物质,所以原子利用率不是100%,故D错误;
故选B.
B.碳酸氢钠不稳定,加热时易分解生成碳酸钠,碳酸钠较稳定,加热时不易分解,所以除去碳酸钠固体中少量NaHCO3可用热分解的方法,故B正确;
C.过氧化尿素的漂白性是利用其强氧化性,二氧化硫的漂白性是利用其和有色物质反应生成无色物质,所以反应原理不同,故C错误;
D.二氧化碳合成甲醇时,除了生成甲醇外还生成其它物质,所以原子利用率不是100%,故D错误;
故选B.
点评:本题涉及反应热、除杂、漂白原理等知识点,难度不大,注意二氧化硫有漂白性,但不能漂白酸碱指示剂,为易错点.

练习册系列答案
相关题目
下列说法中错误的是( )
| A、在NH4+和Fe(CO)5中都存在配位键 |
| B、SO2、SO3都是极性分子 |
| C、元素电负性越大的原子,该元素的原子吸引电子的能力越强 |
| D、离子晶体的晶格能随着离子间距的减少而增大,晶格能越大,晶体的熔点越高 |
将钠投入到滴有酚酞的水中,下列有关叙述中不正确的是( )
| A、产生无色气体 |
| B、Na下沉 |
| C、溶液变红 |
| D、Na块熔化成小球 |
某有机物的氧化产物是甲,还原产物是乙.甲和乙都能与钠反应放出H2,甲和乙反应生成丙,甲和丙都能发生银镜反应.该有机物是( )
| A、甲醛 | B、乙醛 | C、甲酸 | D、甲醇 |
下列物质的分离方法错误的是( )
| A、采用蒸发法从食盐水中提取食盐 |
| B、用结晶法除去硝酸钾中的氯化钠 |
| C、用酒精从溴水中萃取溴 |
| D、用分液法分离汽油和水的混合物 |
如图中所示的实验方法、装置或操作完全正确的是( )
A、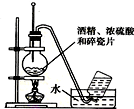 实验室制乙烯 |
B、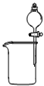 分离苯酚和水 |
C、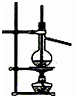 石油的蒸馏 |
D、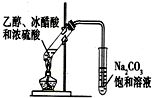 实验室制乙酸乙酯 |