题目内容
14.将一试管(15mL)NO2倒扣于水中,试管中还剩余的气体体积为( )| A. | 10mL | B. | 5mL | C. | 15mL | D. | 0 |
分析 NO2与水反应,发生3NO2+H2O═2HNO3+NO,每3体积NO2反应生成1体积NO,结合反应的方程式计算.
解答 解:NO2与水反应,3NO2+H2O=2HNO3+NO,每3体积NO2反应生成1体积NO,设剩余的气体体积为x,则:
3NO2+H2O=2HNO3+NO
3 1
15mL x
x=5mL,
则剩余气体的体积为5mLNO,
故选B.
点评 本题考查二氧化氮与水的反应,侧重于学生的分析能力和计算能力的考查,明确发生的化学反应,结合方程式计算是解答本题的关键,难度不大.

练习册系列答案
相关题目
4.定量实验是化学的重要组成部分.下列关于学习定量测定的说法中正确的是( )
| A. | 主要学习实验方法,体验一下实验操作即可,不必追求精确 | |
| B. | 应该先做好实验报告,并事先填好,再做实验 | |
| C. | 要实事求是地记录自己的测定结果 | |
| D. | 本组实验失误,实验报告可以参照邻组的结果 |
9. 如图为元紊周期表中短周期非金属元素,W原子最外层电子数是其电子层数的2倍,下列说法不正确的是( )
如图为元紊周期表中短周期非金属元素,W原子最外层电子数是其电子层数的2倍,下列说法不正确的是( )
 如图为元紊周期表中短周期非金属元素,W原子最外层电子数是其电子层数的2倍,下列说法不正确的是( )
如图为元紊周期表中短周期非金属元素,W原子最外层电子数是其电子层数的2倍,下列说法不正确的是( )| A. | 原子半径Y>Z | B. | WZ2能使酸性高锰酸钾溶液褪色 | ||
| C. | X的氢化物比Y的氢化物稳定 | D. | W元素氧化物的水化物一定是强酸 |
19.1g氮气含有m个分子,则阿伏加德罗常数的值可表示为( )
| A. | $\frac{m}{28}$ | B. | m | C. | $\frac{m}{14}$ | D. | 28m |
5. 中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:
中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:
(1)从如图实验装置看,其中尚缺少的一种玻璃用品是环形玻璃搅拌器,除此之外,装置中的一个明显错误是大烧杯杯口与小烧杯杯口没有相平.
(2)若改用60mL 0.25mol•L-1H2SO4和50mL 0.55mol•L-1NaOH溶液进行反应与上述实验相比,所放出的热量不相等(填“相等”、“不相等”),若实验操作均正确,则所求中和热相等(填“相等”“不相等”).
(3)实验数据如表:
①请填写如表中的空白:
②近似认为0.55mol/L NaOH溶液和0.25mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g•℃).则中和热△H=-56.8 kJ/mol (取小数点后一位).
 中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:
中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题:(1)从如图实验装置看,其中尚缺少的一种玻璃用品是环形玻璃搅拌器,除此之外,装置中的一个明显错误是大烧杯杯口与小烧杯杯口没有相平.
(2)若改用60mL 0.25mol•L-1H2SO4和50mL 0.55mol•L-1NaOH溶液进行反应与上述实验相比,所放出的热量不相等(填“相等”、“不相等”),若实验操作均正确,则所求中和热相等(填“相等”“不相等”).
(3)实验数据如表:
①请填写如表中的空白:
| 温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 | 3.4 |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 | |
3.下列离子在溶液中能大量共存的一组是( )
| A. | Na+、Al3+、Cl-、OH- | B. | Na+、H+、OH-、Cl- | ||
| C. | NH4+、Mg2+、SO42-、Cl- | D. | Na+、Cl-、AlO2-、H+ |
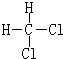 或
或 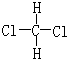
 .氟元素最低负化合价为-1 价.
.氟元素最低负化合价为-1 价. .
.