题目内容
已知BaCO3和BaSO4均为难溶电解质,其溶度积分别为Ksp(BaCO3)=5.1×10-9mol2?L-2,Ksp(BaSO4)=1.1×10-10 mol2?L-2,则下列说法中正确的是( )
| A、BaSO4可做钡餐而BaCO3不能是因为Ksp(BaSO4)<Ksp(BaCO3) |
| B、在制腈纶纤维的1 L溶液中含SO42-为1.0×10-3 mol,则加入0.01 mol BaCl2不能使SO42-完全沉淀 |
| C、在清理有关仪器的BaSO4沉淀时,常加入饱和Na2CO3溶液,使BaSO4转化为BaCO3再用酸处理 |
| D、用稀H2SO4洗涤BaSO4效果比用水好,BaCO3也能用此法处理 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:A.根据BaCO3的溶解平衡:BaCO3?Ba2++CO32-,H+能与CO32-反应生成水和二氧化碳,促进溶解平衡正向移动;
不能代替BaSO4作为“钡餐”的原因
B.当Qc(BaSO4)>Ksp(BaSO4)时,可生成沉淀;
C.难溶电解质的溶解平衡中,溶度积小的电解质也能向溶度积大的电解质转化,注意浓度的大小问题;
D.根据BaSO4的溶解平衡:BaSO4?Ba2++SO42-,H+对于该平衡无影响;
BaCO3?Ba2++CO32-,H+能与CO32-反应生成水和二氧化碳,促进溶解平衡正向移动.
不能代替BaSO4作为“钡餐”的原因
B.当Qc(BaSO4)>Ksp(BaSO4)时,可生成沉淀;
C.难溶电解质的溶解平衡中,溶度积小的电解质也能向溶度积大的电解质转化,注意浓度的大小问题;
D.根据BaSO4的溶解平衡:BaSO4?Ba2++SO42-,H+对于该平衡无影响;
BaCO3?Ba2++CO32-,H+能与CO32-反应生成水和二氧化碳,促进溶解平衡正向移动.
解答:
解:A.因胃酸可与CO32-反应生成水和二氧化碳,使CO32-浓度降低,从而使平衡BaCO3(s)?Ba2+(aq)+CO32-(aq) 向溶解方向移动,使Ba2+浓度增大,Ba2+有毒,与Ksp大小无关,故A错误;
B.已知1L溶液中n(SO42-)=0.001mol,n(Ba2+)=0.01mol,则c(Ba2+)=0.01mol/L,则c(SO42-)=0.001mol/L,Qc(BaSO4)=0.01×0.001=10-5>Ksp(BaSO4)=1.1×10-10,所以能使SO42-完全沉淀,故B错误;
C.常温下,向试管中加入饱和Na2CO3溶液,部分BaSO4因饱和Na2CO3溶液中高浓CO32-转化BaCO3,属于沉淀的转化,碳酸钡能溶于盐酸,故可清洗,故C正确;
D.根据BaSO4的溶解平衡:BaSO4?Ba2++SO42-,H+对于该平衡无影响,硫酸根离子抑制了硫酸钡的溶解;
根据BaCO3的溶解平衡:BaCO3?Ba2++CO32-,H+能与CO32-反应生成水和二氧化碳,促进溶解平衡正向移动;增大了碳酸钡的溶解度,故D错误;
故选C.
B.已知1L溶液中n(SO42-)=0.001mol,n(Ba2+)=0.01mol,则c(Ba2+)=0.01mol/L,则c(SO42-)=0.001mol/L,Qc(BaSO4)=0.01×0.001=10-5>Ksp(BaSO4)=1.1×10-10,所以能使SO42-完全沉淀,故B错误;
C.常温下,向试管中加入饱和Na2CO3溶液,部分BaSO4因饱和Na2CO3溶液中高浓CO32-转化BaCO3,属于沉淀的转化,碳酸钡能溶于盐酸,故可清洗,故C正确;
D.根据BaSO4的溶解平衡:BaSO4?Ba2++SO42-,H+对于该平衡无影响,硫酸根离子抑制了硫酸钡的溶解;
根据BaCO3的溶解平衡:BaCO3?Ba2++CO32-,H+能与CO32-反应生成水和二氧化碳,促进溶解平衡正向移动;增大了碳酸钡的溶解度,故D错误;
故选C.
点评:本题主要考查了溶度积的计算以及溶解平衡的判断及沉淀溶解平衡的应用,难度不大,根据课本知识即可完成.

练习册系列答案
相关题目
下列关于“物质的量”、“摩尔”和“摩尔质量”的叙述中正确的是( )
| A、0.012kg12C中所含的碳原子数为NA |
| B、“物质的量”是国际单位制中的一个基本单位 |
| C、物质的摩尔质量等于其相对分子(原子)质量 |
| D、1mol任何物质都含有约6.02×1023个原子 |
下列颜色不属于因化学反应而产生的现象的是( )
| A、无色试剂瓶中的浓硝酸呈黄色 |
| B、白色硫酸铜粉末在空气中变成蓝色 |
| C、鸡蛋白遇浓硝酸呈黄色 |
| D、普通玻璃导管口点燃纯净氢气时,火焰呈黄色 |
下列事实与胶体知识有关的是( )
①用盐卤制豆腐
②用明矾净水
③河海交接处易形成沙洲
④一支钢笔使用不同牌号的蓝黑墨水易堵塞
⑤工厂静电除尘.
①用盐卤制豆腐
②用明矾净水
③河海交接处易形成沙洲
④一支钢笔使用不同牌号的蓝黑墨水易堵塞
⑤工厂静电除尘.
| A、①②⑤ | B、①③④⑤ |
| C、①②③④⑤ | D、都无关 |
下列说法不正确的是 ( )
| A、用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小 |
| B、物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的 |
| C、对于Al(OH)3(s)?Al(OH)3(aq)?Al3++3OH-,前者为溶解平衡,后者为电离平衡 |
| D、除溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3大 |
| E、沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全 |
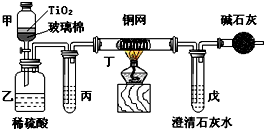 电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol?L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞.回答下列问题:
电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol?L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞.回答下列问题: 大气中的部分碘源于O3对海水中I-的氧化.将O3持续通入NaI酸性溶液溶液中进行模拟研究.
大气中的部分碘源于O3对海水中I-的氧化.将O3持续通入NaI酸性溶液溶液中进行模拟研究.
 已知:①将煤转化为水煤气的主要化学反应为C(s)+H2O(g)
已知:①将煤转化为水煤气的主要化学反应为C(s)+H2O(g)