题目内容
1.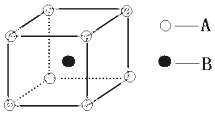 根据离子晶体的晶胞结构,判断下列离子晶体的化学式:AB(A表示阳离子,B表示阴离子).
根据离子晶体的晶胞结构,判断下列离子晶体的化学式:AB(A表示阳离子,B表示阴离子).
分析 根据均摊法计算,由晶胞的结构图可知,B子分布在晶胞的体心,数目为1,A原子分布在晶胞的顶点上,数目为8×$\frac{1}{8}$=1,由此解得化学式.
解答 解:由晶胞的结构图可知,B子分布在晶胞的体心,数目为1,A原子分布在晶胞的顶点上,数目为8×$\frac{1}{8}$=1,所以化学式为AB,故答案为:AB.
点评 本题考查了利用均摊法计算晶胞的化学式的方法,难度较小,解题时仔细观察晶胞的结构图即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列物质不能把含有酸性Fe2+的溶液氧化成Fe3+的是( )
| A. | 新制氯水 | B. | 酸性高锰酸钾溶液 | ||
| C. | 往溶液中通入氧气 | D. | 往溶液中加入铁粉 |
16.有两种二元弱酸H2A与H2B.酸性强弱顺序为:酸性强弱顺序H2A>H2B>HA->HB-,(已知:H2A.Ka1=1.54×10-2,Ka2=1.02×10-2),下列说法正确的是( )
| A. | 等浓度等体积H2A与NaOH的混合溶液呈碱性 | |
| B. | H2A与少量B2-反应的离子方程式为2H2A+B2-=2HA-+H2B | |
| C. | NaHB溶液一定显酸性 | |
| D. | 等浓度等体积的NaHA与Na2B混合,混合溶液中存在这样的关系:c(A2-)>c(B2-)>c(HA-)>c(HB-) |
6.化学平衡常数可以用K来表示,下列关于化学平衡常数的说法中正确的是( )
| A. | K越大,反应物的转化率越小 | B. | K与反应物的浓度有关 | ||
| C. | K与生成物的浓度有关 | D. | K与温度有关 |
13.已知:4NH3(g)+3O2(g)═2N2(g)+6H2O(g)△H=-1269kJ/mol下列说法正确的是( )
| A. | 断开1 mol O-O键比断开1 mol N-N键所需能量少448 kJ | |
| B. | 断开1 mol H-O键比断开1 mol H-N键所需能量相差约72.6 kJ | |
| C. | 由以上键能的信息可知H2O的沸点比NH3高 | |
| D. | 由元素非金属性的强弱可知 H-O键比H-N键弱 |
10.下列物质属于电解质的是( )
| A. | 氨水 | B. | 食醋 | C. | 胆矾 | D. | 酒精 |