题目内容
7.短周期元素甲、乙、丙、丁的原子序数依次增大,甲原子核外最外层电子数为内层电子数的3倍,丁原子的核电荷数是甲原子核电荷数的2倍,乙、丙、丁最高价氧化物对应的水化物两两之间能相互反应.下列说法错误的是( )| A. | 元素丙的单质可用于冶炼金属 | B. | 甲与丁形成的分子是酸性氧化物 | ||
| C. | 简单离子半径:丁>乙>丙 | D. | 甲与乙形成的化合物均有强氧化性 |
分析 短周期元素甲、乙、丙、丁的原子序数依次增大,甲原子核外最外层电子数为内层电子数的3倍,则甲含有2个电子层,最外层含有6个电子,为O元素;丁原子的核电荷数是甲原子核电荷数的2倍,则丁的核电荷数是16,为S元素;乙、丙、丁最高价氧化物对应的水化物两两之间能相互反应,则乙为Na、丙为Al元素,据此进行解答.
解答 解:短周期元素甲、乙、丙、丁的原子序数依次增大,甲原子核外最外层电子数为内层电子数的3倍,则甲含有2个电子层,最外层含有6个电子,为O元素;丁原子的核电荷数是甲原子核电荷数的2倍,则丁的核电荷数是16,为S元素;乙、丙、丁最高价氧化物对应的水化物两两之间能相互反应,则乙为Na、丙为Al元素,
A.丙为Al,金属铝可以通过铝热反应冶炼金属,故A正确;
B.甲与丁形成的化合物为二氧化硫、三氧化硫,二者都是酸性氧化物,故B正确;
C.离子的电子层越多,离子半径越大,电子层相同时,核电荷数越大,离子半径越小,则离子半径大小为:丁>乙>丙,故C正确;
D.甲、乙分别为O、Na,二者形成的化合物为氧化钠、过氧化钠,氧化钠不具有强氧化性,故D错误;
故选C.
点评 本题考查了原子结构与元素周期律的关系,题目难度中等,推断元素为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
17.某实验小组为测定工业纯碱中碳酸钠的质量分数(含少量NaCl),准确称量wg样品进行实验,下列实验方法所对应的实验方案和测量数据最合理的是( )
| 实验方法 | 实验方案 | 测量数据 | |
| A | 滴定法 | 将样品配成100mL溶液,取10.00mL,加人甲基橙,用标准盐酸滴定 | 消耗盐酸的体积 |
| B | 量气法 | 将样品与盐酸反应,使生成的气体全部被碱石灰吸收 | 碱石灰增重 |
| C | 重量法 | 将样品放人烧杯中,置于天平上,加入足量盐酸 | 减轻的质量 |
| D | 量气法 | 将样品与盐酸反应,气体通过排水量气装置量气 | 排水体积 |
| A. | A | B. | B | C. | C | D. | D |
18.X原子的最外层电子的排布为ns2np5,则X的氢化物的化学式是( )
| A. | HX | B. | H2X | C. | XH3 | D. | XH4 |
16.以下有关物质结构的描述正确的是( )
| A. | 甲苯分子中的所有原子可能共平面 | |
| B. | 苯乙烯分子中的所有原子可能共平面 | |
| C. | 二氯甲烷分子为正四面体结构 | |
| D. | 丁烷分子中的所有碳原子不可能都在同一平面内 |
17.已知A、B、C、D的原子序数都不超过18,它们的离子aA(n+1)+、bBn+、cC(n+1)-、dDn-均具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子序数:a>b>c>d | |
| B. | 离子半径:A(n+1)+>Bn+>C(n+1)->Dn- | |
| C. | 离子还原性:A(n+1)+>Bn+,离子氧化性:C(n+1)->Dn- | |
| D. | 单质还原性:B>A,单质氧化性:D>C |
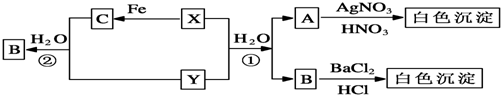
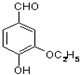 是食品添加剂的增香原料,其香味比香草醛更浓郁.
是食品添加剂的增香原料,其香味比香草醛更浓郁.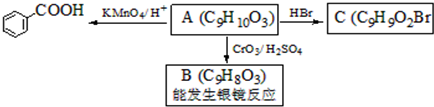
 ,属于取代反应(填反应类型).
,属于取代反应(填反应类型). .
. .
.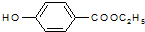 )是一种医药中间体,请设计合理方案用
)是一种医药中间体,请设计合理方案用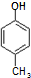 合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).
合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).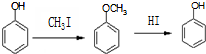
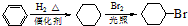
 .
.