题目内容
13.为了除去KCl溶液中少量的MgCl2、MgS04,从稀盐酸、Na2C03、Ba(N03)2、K2CO3、Ba(OH)2溶液中,选择A、B、C三种试剂,按图中的实验步骤进行換作:溶液$→_{过滤}^{加过量A后}$滤液$→_{过滤}^{加过量B后}$滤液$\stackrel{加适量C}{→}$较纯净的KCl溶液
(1)试剂的化学式:ABa(OH)2,BK2CO3,CHCl
(2)加过量A的原因是为了除尽Mg2+和SO42-有关反应的离子方程式为Mg2++2OH-=Mg(OH)2↓、Ba2++SO42-=BaSO4↓
(3)加过量B的原因是为了除尽过量的Ba2+有关反应的离子方程式为Ba2++CO32-=BaCO3↓
(4)加适量C的作用是将KOH转化为KCl,同时除去过量的K2CO3.
分析 除去KCl溶液中的少量MgCl2和MgSO4,可看成把Mg2+、SO42-沉淀而除去,因此选择所提供试剂中的Ba(OH)2可同时沉淀掉Mg2+、SO42-离子;反应生成的BaCl2和过量的Ba(OH)2以及原有的MgCl2可加入所选试剂中的K2CO3而除去;最后通过滴加盐酸可把过量的K2CO3及反应生成的KOH同时反应掉而生成KCl,将KCl溶液进行蒸发操作可得到KCl,以此解答该题.
解答 解:除去KCl溶液中的少量MgCl2和MgSO4,可看成把Mg2+、SO42-沉淀而除去,因此选择所提供试剂中的Ba(OH)2可同时沉淀掉Mg2+、SO42-离子;反应生成的BaCl2和过量的Ba(OH)2以及原有的MgCl2可加入所选试剂中的K2CO3而除去;最后通过滴加盐酸可把过量的K2CO3及反应生成的KOH同时反应掉而生成KCl,将KCl溶液进行蒸发操作可得到KCl,
(1)由以上分析可知A为Ba(OH)2、B为K2CO3、C为HCl,故答案为:Ba(OH)2、K2CO3、HCl;
(2)为确保混合溶液中的MgCl2和MgSO4全部反应而沉淀掉,应加入过量的Ba(OH)2,生成Mg(OH)2、BaSO4;反应的离子方程式为:Mg2++2OH-=Mg(OH)2↓ Ba2++SO42-=BaSO4↓;
故答案为:为了除尽Mg2+和SO42-;Mg2++2OH-=Mg(OH)2↓、Ba2++SO42-=BaSO4↓;
(3)为确保溶液是的Ba2+全部沉淀而除去,应加入过量的K2CO3到沉淀不再产生;反应生成碳酸钡沉淀、氯化钾、氢氧化钾;反应的离子方程式为:Ba2++CO32-=BaCO3↓;
故答案为:为了除尽过量的Ba2+;Ba2++CO32-=BaCO3↓;
(4)加入过量碳酸钾后,溶液中含有氯化钾、氢氧化钾、碳酸钾,为得到纯净的氯化钾,应加入盐酸,将KOH转化为KCl,同时除去过量的K2CO3,
故答案为:将KOH转化为KCl,同时除去过量的K2CO3.
点评 本题考查物质的分离、提纯知识,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握实验的原理和操作方法,为解答该题的关键,难度不大.

| A. | 氢氧燃料电池的正极反应式为H2+2OH--2e-═2H2O | |
| B. | 用铂电极电解硫酸铜溶液的阳极反应式为4OH--4e-═O2↑+2H2O | |
| C. | 表示醋酸与NaOH的稀溶液反应的中和热的化学方程式为H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ.mol-1 | |
| D. | NaHSO3溶于水时水解的离子方程式为HSO3-+H2O?SO32-+H3O+ |
| A. | a>b>c | B. | c>a>b | C. | b>a>c | D. | a>c>b |
| A. | 镁条燃烧可用泡沫灭火器灭火 | |
| B. | 工业上电解氯化钠、氯化镁溶液制取可以得到金属钠、镁 | |
| C. | 通常情况下,铁是银白色金属,硬度较大,可以被磁石吸引 | |
| D. | 铜能与氯化铁溶液反应,该反应可以用于印刷电路板的制作 |
| A. | 原子半径:W>Z>Y | |
| B. | 元素W最高价氧化物的水化物为强酸 | |
| C. | 化合物X2Y、Z2Y中化学键的类型相同 | |
| D. | 元素Y的简单气态氢化物的热稳定性比W的弱 |
| A. | C2H5Br和NaOH溶液混合共热 | |
| B. | 乙醇和NaOH溶液混合共热 | |
| C. | 一溴丁烷与的NaOH的丁醇溶液混合共热 | |
| D. | 氯苯与NaOH溶液混合共热 |
| A. | CuSO4溶液 | B. | Na2CO3溶液 | C. | Fe(OH)3胶体 | D. | Ba(OH)2溶液 |
| A. | Mg(OH)2不溶于水,但能溶于浓NH4Cl溶液中 | |
| B. | 水垢中含有的CaSO4,先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3,再用酸除去 | |
| C. | 洗涤BaSO4沉淀时,用稀硫酸洗涤BaSO4沉淀比用蒸馏水洗涤损失少 | |
| D. | FeCl3溶液中混有FeCl2,常加入少量的H2O2,使Fe2+氧化为Fe3+ |
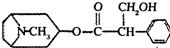
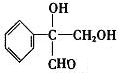 或
或 ;
;