��Ŀ����
���ܱ������У���1.0mol CO��1.0mol H2O��ϼ��ȵ�800�棬�������з�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g����һ��ʱ���÷�Ӧ�ﵽƽ�⣬���CO�����ʵ���Ϊ0.5mol��������˵����ȷ���ǣ�������
| A��800���£��÷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ0.25 |
| B��427��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ9.4����÷�Ӧ�ġ�H��0 |
| C��800���£����������ƽ����ϵ��ͨ��1.0 mol��CO��g������ƽ��ʱCO���ʵ�������Ϊ33.3% |
| D��800���£����������ƽ����ϵ��ͨ��1.0 mol��H2O��g������ƽ��ʱCOת����Ϊ66.7% |
���㣺��ѧƽ��ļ���
ר�⣺��ѧƽ��ר��
������A������CO�����ʵ�������������ʽ����ƽ��ʱ����ֵ����ʵ��������ڷ�Ӧǰ�������������䣬�����ʵ�ϵ��Ϊ1���ʿ��������ʵ�������Ũ�ȴ���ƽ�ⳣ������ʽ���㣻
B�����A�е�ƽ�ⳣ�����жϽ����¶�ƽ����ƶ����ݴ��жϷ�Ӧ��ЧӦ��
C��800���£����������ƽ����ϵ��ͨ��1.0 mol��CO��g������ЧΪ��ʼ����2.0mol CO��1.0mol H2O����ƽ��ʱ�μӷ�Ӧ��CO�����ʵ���Ϊbmol����������ʽ��ʾ��ƽ��ʱ����ֵ����ʵ���������ƽ�ⳣ���з��̼���b��ֵ���ٸ���ת���ʶ�����㣮
D��800���£����������ƽ����ϵ��ͨ��1.0 mol��H2O��g������ЧΪ��ʼ����1.0mol CO��2.0mol H2O����ƽ��ʱ�μӷ�Ӧ��CO�����ʵ���Ϊamol����������ʽ��ʾ��ƽ��ʱ����ֵ����ʵ���������ƽ�ⳣ���з��̼���a��ֵ���ٸ���ת���ʶ�����㣻
B�����A�е�ƽ�ⳣ�����жϽ����¶�ƽ����ƶ����ݴ��жϷ�Ӧ��ЧӦ��
C��800���£����������ƽ����ϵ��ͨ��1.0 mol��CO��g������ЧΪ��ʼ����2.0mol CO��1.0mol H2O����ƽ��ʱ�μӷ�Ӧ��CO�����ʵ���Ϊbmol����������ʽ��ʾ��ƽ��ʱ����ֵ����ʵ���������ƽ�ⳣ���з��̼���b��ֵ���ٸ���ת���ʶ�����㣮
D��800���£����������ƽ����ϵ��ͨ��1.0 mol��H2O��g������ЧΪ��ʼ����1.0mol CO��2.0mol H2O����ƽ��ʱ�μӷ�Ӧ��CO�����ʵ���Ϊamol����������ʽ��ʾ��ƽ��ʱ����ֵ����ʵ���������ƽ�ⳣ���з��̼���a��ֵ���ٸ���ת���ʶ�����㣻
���
�⣺A��ƽ��ʱCO�����ʵ���Ϊ0.5mol����
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ��mol����1 1 0 0
�仯��mol����0.5 0.5 0.5 0.5
ƽ�⣨mol����0.5 0.5 0.5 0.5
�ʸ��¶���ƽ�ⳣ��k=
=1����A����
B��427��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ9.4������800��ʱ��ƽ�ⳣ��1���ʽ����¶�ƽ��������Ӧ���У��÷�Ӧ����Ӧ�Ƿ��ȷ�Ӧ������H��0����B����
C��800���£����������ƽ����ϵ��ͨ��1.0 mol��CO��g������ЧΪ��ʼ����2.0mol CO��1.0mol H2O����ƽ��ʱ�μӷ�Ӧ��CO�����ʵ���Ϊbmol����
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ��mol����2 1 0 0
�仯��mol����b b b b
ƽ�⣨mol����2-b 1-b b b
����
=1�����b=
����CO����������=
��100%=
��100%=44.4%����C����
D��800���£����������ƽ����ϵ��ͨ��1.0 mol��H2O��g������ЧΪ��ʼ����1.0mol CO��2.0mol H2O����ƽ��ʱ�μӷ�Ӧ��CO�����ʵ���Ϊamol����
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ��mol����1 2 0 0
�仯��mol����a a a a
ƽ�⣨mol����1-a 2-a a a
����
=1�����a=
����CO��ת����Ϊ
��100%=66.7%����D��ȷ��
��ѡD��
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ��mol����1 1 0 0
�仯��mol����0.5 0.5 0.5 0.5
ƽ�⣨mol����0.5 0.5 0.5 0.5
�ʸ��¶���ƽ�ⳣ��k=
| 0.5��0.5 |
| 0.5��0.5 |
B��427��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ9.4������800��ʱ��ƽ�ⳣ��1���ʽ����¶�ƽ��������Ӧ���У��÷�Ӧ����Ӧ�Ƿ��ȷ�Ӧ������H��0����B����
C��800���£����������ƽ����ϵ��ͨ��1.0 mol��CO��g������ЧΪ��ʼ����2.0mol CO��1.0mol H2O����ƽ��ʱ�μӷ�Ӧ��CO�����ʵ���Ϊbmol����
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ��mol����2 1 0 0
�仯��mol����b b b b
ƽ�⣨mol����2-b 1-b b b
����
| b��b |
| (2-b)(1-b) |
| 2 |
| 3 |
| 2-b |
| 3 |
2-
| ||
| 3 |
D��800���£����������ƽ����ϵ��ͨ��1.0 mol��H2O��g������ЧΪ��ʼ����1.0mol CO��2.0mol H2O����ƽ��ʱ�μӷ�Ӧ��CO�����ʵ���Ϊamol����
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ��mol����1 2 0 0
�仯��mol����a a a a
ƽ�⣨mol����1-a 2-a a a
����
| a��a |
| (1-a)(2-a) |
| 2 |
| 3 |
| ||
| 1mol |
��ѡD��
���������⿼�黯ѧƽ�ⳣ�����йؼ��㣬�Ѷ��еȣ�ע�⻯ѧƽ�ⳣ������;��1���жϷ�Ӧ���еij̶ȣ�2���жϷ�Ӧ����ЧӦ��3���жϷ�Ӧ���еķ���4������ת���ʣ�

��ϰ��ϵ�д�
 ���ɶ��ȫ���ƿؾ�ϵ�д�
���ɶ��ȫ���ƿؾ�ϵ�д�
�����Ŀ
���������Ʊ������漰�ķ�Ӧ�У����������ӷ�Ӧ���ǣ�������
| A������������NaOH��Һ�� |
| B��NaAlO2��Һ���ữ |
| C������������������ |
| D��������ڵ������� |
��4L�ܱ������г���6molA�����5molB���壬��һ�������·�����Ӧ��3A��g��+B��g��?2C��g��+xD��g�����ﵽƽ��ʱ��������2molC�����ⶨD��Ũ��Ϊ0.5mol?L-1�����ж���ȷ���ǣ�������
| A��x=1 |
| B���ﵽƽ��ʱ������ͬ�¶��������ڻ�������ѹǿ�Ƿ�Ӧǰ��8.5�� |
| C��ƽ��ʱA��Ũ��Ϊ1.50?L-1 |
| D��B��ת����Ϊ20% |
����ʵ������л��Ȳ�����ɫ������������ܽ���ǣ�������
| A����AlCl3��Һ�еμӰ�ˮ������ |
| B����Ba��NO3��2��Һͨ��SO2������ |
| C����Ba��0H��2��Һͨ��CO2������ |
| D��������Fe��OH��3�����еμ�ϡ���������� |
������˪��As2O3����������п�������Ϸ�Ӧ�����ɵ��黯�⣨AsH3�����Ȳ���������ȫ�ֽ�ɵ���������������������Ϊ1.50g��������
| A������������˪Ϊ1.98 g |
| B���ֽ����������Ϊ672 mL |
| C������˪��Ӧ��пΪ3.90 g |
| D��ת�Ƶĵ�������Ϊ0.06NA |

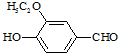 ����ʳƷ���Ӽ�������ԭ�ϣ�����ζ�����ȩ����Ũ����
����ʳƷ���Ӽ�������ԭ�ϣ�����ζ�����ȩ����Ũ����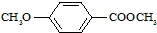 ����һ��ҽҩ�м��壬����ƺ�������������ȩ��
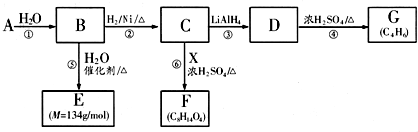
����һ��ҽҩ�м��壬����ƺ�������������ȩ�� 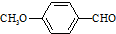 ���ϳ�X���÷�Ӧ����ͼ��ʾ���£�
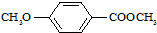
���ϳ�X���÷�Ӧ����ͼ��ʾ���£�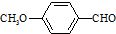 ��
��
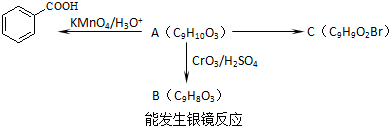
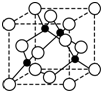 A��B��C��D��E��F��Ϊ���ڱ���ǰ������Ԫ�أ���ԭ������������������A��B��CΪ�����ڷǽ���Ԫ�أ�A���γɻ�������������Ԫ�أ�Bԭ�ӻ�̬�����Ų���ֻ��һ��δ�ɶԵ��ӣ�C��ͬ����Ԫ����ԭ�Ӱ뾶��С��Ԫ�أ���B��Cͬ���壮D�Ļ�̬ԭ����ǰ������Ԫ�صĻ�̬ԭ���е���������ࣻE ��D���ڣ�E��ij��������X��C���⻯���Ũ��Һ����ʱ��Ӧ������ʵ������ȡ��̬����C��F��D��������������ȣ�
A��B��C��D��E��F��Ϊ���ڱ���ǰ������Ԫ�أ���ԭ������������������A��B��CΪ�����ڷǽ���Ԫ�أ�A���γɻ�������������Ԫ�أ�Bԭ�ӻ�̬�����Ų���ֻ��һ��δ�ɶԵ��ӣ�C��ͬ����Ԫ����ԭ�Ӱ뾶��С��Ԫ�أ���B��Cͬ���壮D�Ļ�̬ԭ����ǰ������Ԫ�صĻ�̬ԭ���е���������ࣻE ��D���ڣ�E��ij��������X��C���⻯���Ũ��Һ����ʱ��Ӧ������ʵ������ȡ��̬����C��F��D��������������ȣ�