题目内容
3.下列化学方程式或离子方程式正确的是( )| A. | 将Al条投入NaOH溶液中:Al+OH-+H2O═[Al(OH)4]-+H2↑ | |
| B. | 向氯化铵的稀溶液中加入少量NaOH NH4++OH-═NH3↑+H2O | |
| C. | 浓盐酸与铁屑反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 向浓硝酸中加入铜片Cu+4H++2N03-═Cu2++2NO2↑+2H2O |
分析 A.电子不守恒;
B.少量NaOH,生成氯化钠、一水合氨;
C.反应生成氯化亚铁和氢气;
D.发生氧化还原反应,遵循电子、电荷守恒.
解答 解:A.将Al条投入NaOH溶液中的离子反应为2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑,故A错误;
B.向氯化铵的稀溶液中加入少量NaOH的离子反应为NH4++OH-═NH3.H2O,故B错误;
C.浓盐酸与铁屑反应的离子反应为Fe+2H+═Fe2++H2↑,故C错误;
D.向浓硝酸中加入铜片的离子反应为Cu+4H++2N03-═Cu2++2NO2↑+2H2O,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、复分解反应的离子反应及分析与应用能力的考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列物质不能通过化合反应得到的是( )
| A. | Fe (OH)3 | B. | FeCl2 | C. | FeS | D. | Al(OH)3 |
15.如下图所示警示标记中,放浓硫酸的试剂瓶上应印有的( )
| A. |  | B. |  | C. |  | D. |  |
12.铝、铍(Be)及其化合物具有相似的化学性质,如其氯化物分子内键型相同,故其氯化物晶体的熔点都较低.已知反应:BeCl2+Na2BeO2+2H2O═2NaCl+2Be(OH)2↓能完全进行,则下列推断正确的是( )
| A. | Na2BeO2溶液的pH>7,将其蒸干并灼烧后得到的残留物为BeO | |
| B. | BeCl2溶液的pH<7,将其蒸干并灼烧后得到的残留物可能是BeO | |
| C. | Be(OH)2只能溶于盐酸,不能溶于NaOH溶液 | |
| D. | BeCl2水溶液的导电性强,故BeCl2是离子化合物 |
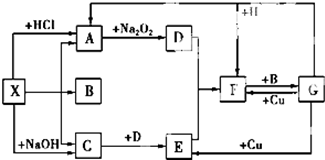 如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出.常温下X和H是固体,B和G是液体,其余均为气体,1molX分解得到A、B、C各1mol.试回答下列各题:
如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出.常温下X和H是固体,B和G是液体,其余均为气体,1molX分解得到A、B、C各1mol.试回答下列各题: