题目内容
1.下列反应的离子方程式正确的是( )| A. | NaHCO3溶液与盐酸:CO32-+2 H+═H2O+CO2↑ | |
| B. | 向澄清的石灰水中加入过量的小苏打溶液:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| C. | 向硝酸亚铁溶液中加入稀硫酸:Fe2++4H++NO3-═Fe3++NO↑+2H2O | |
| D. | AlCl3溶液与过量氨水反应:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
分析 A.碳酸氢根离子不能拆开;
B.小苏打为碳酸氢钠,碳酸氢钠过量,反应生成碳酸钙沉淀、碳酸钠和水;
C.离子方程式两边正电荷不相等,违反了电荷守恒;
D.氨水为弱碱,无法弱碱氢氧化铝,二者反应生成氢氧化铝沉淀;
解答 解:A.NaHCO3溶液与盐酸生成氯化钠和水,正确的离子方程式为:HCO3-+H+═H2O+CO2↑,故A错误;
B.向澄清的石灰水中加入过量的小苏打溶液,反应生成碳酸钠、碳酸钙沉淀和水,反应的离子方程式为:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32-,故B正确;
C.向硝酸亚铁溶液中加入稀硫酸,二者发生氧化还原反应,正确的离子方程式为:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O,故C错误;
D.AlCl3溶液与过量氨水反应生成氢氧化铝沉淀和氯化铵,正确的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故D错误;
故选B.
点评 本题考查了离子方程式的书写判断,题目难度不大,注意掌握离离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案
相关题目
4. 文艺复兴时期,群青颜料曾用在许多著名的油画上,当时群青颜料是由贵重的青金石研磨并制成的.青金石是指碱性铝硅酸盐矿物,其中含钠、铝、硅、硫、氯、氧等元素.
文艺复兴时期,群青颜料曾用在许多著名的油画上,当时群青颜料是由贵重的青金石研磨并制成的.青金石是指碱性铝硅酸盐矿物,其中含钠、铝、硅、硫、氯、氧等元素.
(1)硅元素基态原子的价电子轨道表示式为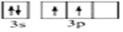 .
.
(2)第四周期中,与铝未成对电子数相同的金属元素有4种.
(3)Na+和Ne互为等电子体,电离能I2(Na)> I1(Ne)(填“>”或“<”).
(4)①已知氯有多种含氧酸,其电离平衡常数如下:
HClO4的结构简式为 ,HClO3中Cl原子的杂化轨道类型为sp3,HClO2中含有的共价键类型为σ键和π键.以上几种含氧酸的酸性强弱不同,其原因为几种含氧酸的酸性强弱不同,其原因为.
,HClO3中Cl原子的杂化轨道类型为sp3,HClO2中含有的共价键类型为σ键和π键.以上几种含氧酸的酸性强弱不同,其原因为几种含氧酸的酸性强弱不同,其原因为.
②氢卤酸(HX)的电离过程如图.△H1和△H2的递变规律都是HF>HCl>HBr>HI,其中△H1(HF)特别大的原因为HF分子与水分子间存在氢键,电离时需要更多能量,影响△H2递变的因素为键能.
(5)铝单质为面心立方晶体,晶胞参数a=q nm,铝的摩尔质量为Mg•mol-1,原子半径为r pm,阿伏伽德罗常数的值为NA.则铝单质的密度为$\frac{4M}{{N}_{A}×{q}^{3}×1{0}^{-21}}$ g•cm-3(列式即可,下同),铝晶胞中原子的体积占晶胞体积的百分率为$\frac{4×\frac{4}{3}π{r}^{3}}{{q}^{3}×1{0}^{9}}$.
 文艺复兴时期,群青颜料曾用在许多著名的油画上,当时群青颜料是由贵重的青金石研磨并制成的.青金石是指碱性铝硅酸盐矿物,其中含钠、铝、硅、硫、氯、氧等元素.
文艺复兴时期,群青颜料曾用在许多著名的油画上,当时群青颜料是由贵重的青金石研磨并制成的.青金石是指碱性铝硅酸盐矿物,其中含钠、铝、硅、硫、氯、氧等元素.(1)硅元素基态原子的价电子轨道表示式为
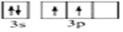 .
.(2)第四周期中,与铝未成对电子数相同的金属元素有4种.
(3)Na+和Ne互为等电子体,电离能I2(Na)> I1(Ne)(填“>”或“<”).
(4)①已知氯有多种含氧酸,其电离平衡常数如下:
| 化学式 | HClO4 | HClO3 | HClO2 | HClO |
| Ka | 1×1010 | 1×101 | 1×10-2 | 4×10-8 |
 ,HClO3中Cl原子的杂化轨道类型为sp3,HClO2中含有的共价键类型为σ键和π键.以上几种含氧酸的酸性强弱不同,其原因为几种含氧酸的酸性强弱不同,其原因为.
,HClO3中Cl原子的杂化轨道类型为sp3,HClO2中含有的共价键类型为σ键和π键.以上几种含氧酸的酸性强弱不同,其原因为几种含氧酸的酸性强弱不同,其原因为.②氢卤酸(HX)的电离过程如图.△H1和△H2的递变规律都是HF>HCl>HBr>HI,其中△H1(HF)特别大的原因为HF分子与水分子间存在氢键,电离时需要更多能量,影响△H2递变的因素为键能.
(5)铝单质为面心立方晶体,晶胞参数a=q nm,铝的摩尔质量为Mg•mol-1,原子半径为r pm,阿伏伽德罗常数的值为NA.则铝单质的密度为$\frac{4M}{{N}_{A}×{q}^{3}×1{0}^{-21}}$ g•cm-3(列式即可,下同),铝晶胞中原子的体积占晶胞体积的百分率为$\frac{4×\frac{4}{3}π{r}^{3}}{{q}^{3}×1{0}^{9}}$.
12.下列关于铁元素的叙述中正确的是( )
| A. | 2Fe3++Cu=2Fe2++Cu2+成立说明氧化性:Fe3+>Cu2+ | |
| B. | 25℃,pH=0的溶液中,Al3+、NH4+、NO3-、Fe2+可以大量共存 | |
| C. | 5.6g铁与足量的氯气反应失去电子为0.2mol | |
| D. | 硫酸铁溶液中加入铁粉,滴加KSCN溶液一定不变血红色 |
16.在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是( )
| A. | Na+、K+、NO3-、Cl- | B. | Na+、Fe2+、SO42-、NO3- | ||
| C. | Cu2+、Na+、SO42-、OH- | D. | Ba2+、SO32-、NO3-、K+ |
6.下列实验操作正确的是( )
| A. | Ba(NO3)2溶于水,可将含有Ba(NO3)2的废液倒入水槽中,再用水冲入下水道 | |
| B. | 取用细口瓶里的试液时,先拿下瓶塞,倒放在桌上,然后标签朝外拿起瓶子,瓶口要紧挨着试管口,将液体缓缓地倒入试管 | |
| C. | 胶头滴管取完一种试液后,可直接取另一种不与其反应的试液 | |
| D. | 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶 |
13.取稀硫酸900克,平均分成6份,分别加入镁粉进行6次实验,记录如表:
(1)表中m1=10;m2=18.
(2)这种稀硫酸中溶质的质量分数是多少?
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 |
| 加入镁粉的质量/克 | 1 | 2 | 3 | 4 | 5 | 6 |
| 生成硫酸镁的质量/克 | 5 | m1 | 15 | 18 | m2 | 18 |
(2)这种稀硫酸中溶质的质量分数是多少?
10.下列溶液中,跟100ml0.5moL/LNaCl溶液所含的Cl-的物质的量浓度相同的是( )
| A. | 100mL0.5mol/LMgCl2溶液 | B. | 200mL0.25mol/LCaCl2溶液 | ||
| C. | 50mL1mol/LNaCl 溶液 | D. | 25mL0.5mol/LAlCl3溶液 |
11. 恒温恒容装置中发生如下反应:A(g)+2B(g)?2C(g)△H=-a kJ•mol-1(a>0),开始时充入一定量的A和B,B的反应速率随时间变化如图所示.下列说法正确是( )
恒温恒容装置中发生如下反应:A(g)+2B(g)?2C(g)△H=-a kJ•mol-1(a>0),开始时充入一定量的A和B,B的反应速率随时间变化如图所示.下列说法正确是( )
 恒温恒容装置中发生如下反应:A(g)+2B(g)?2C(g)△H=-a kJ•mol-1(a>0),开始时充入一定量的A和B,B的反应速率随时间变化如图所示.下列说法正确是( )
恒温恒容装置中发生如下反应:A(g)+2B(g)?2C(g)△H=-a kJ•mol-1(a>0),开始时充入一定量的A和B,B的反应速率随时间变化如图所示.下列说法正确是( )| A. | 反应放出的热量一定小于a kJ | |
| B. | 5s后,反应停止,各物质浓度保持不变 | |
| C. | 5s末,ν(A):ν(B)=1:2 | |
| D. | 阴影部分面积可以表示A的物质的量浓度减少量 |