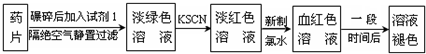
题目内容
下列各项中表达正确的是( )
A、F-的结构示意图: |
B、CO2的分子模型示意图: |
C、NaCl的电子式: |
| D、Cr的外围电子排布式3d44s2 |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.氟离子的核电荷数为9,核外电子总数为10,最外层达到8电子稳定结构;
B.二氧化碳为直线型结构,不是V型;
C.氯化钠为离子化合物,电子式中没有标出阴阳离子所带电荷;
D.Cr的外围电子呈3d′54s1时,3d、4s轨道上的电子处于半满状态,整个体系的能量最低.
B.二氧化碳为直线型结构,不是V型;
C.氯化钠为离子化合物,电子式中没有标出阴阳离子所带电荷;
D.Cr的外围电子呈3d′54s1时,3d、4s轨道上的电子处于半满状态,整个体系的能量最低.
解答:
解:A.氟离子的核电荷数为9,最外层达到8电子稳定结构,氟离子的结构示意图为: ,故A正确;
,故A正确;
B.二氧化碳分子为直线型结构,二氧化碳正确的比例模型为: ,故B错误;
,故B错误;
C.氯化钠属于离子化合物,钠离子直接用离子符号表示,氯离子需要标出最外层电子及所带电荷,氯化钠正确的电子式为: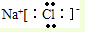 ,故C错误;
,故C错误;
D.3d44s2违背了半充满或全满时为稳定状态,所以Cr的外围电子排布式为3d54s1,故D错误;
故选A.
 ,故A正确;
,故A正确;B.二氧化碳分子为直线型结构,二氧化碳正确的比例模型为:
 ,故B错误;
,故B错误;C.氯化钠属于离子化合物,钠离子直接用离子符号表示,氯离子需要标出最外层电子及所带电荷,氯化钠正确的电子式为:
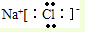 ,故C错误;
,故C错误;D.3d44s2违背了半充满或全满时为稳定状态,所以Cr的外围电子排布式为3d54s1,故D错误;
故选A.
点评:本题考查了常见化学用语的书写判断,题目难度中等,注意掌握比例模型、原子结构示意图、电子式、电子排布式等化学用语的概念及书写原则,明确比例模型与球棍模型、离子结构示意图与原子结构示意图、离子化合物与共价化合物的电子式的区别.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在给定的溶液中,加入对应的一组离子,则该组离子能在原溶液中大量共存的是( )
| A、滴加甲基橙显红色的溶液:I-、NH4+、Cl-、NO3- |
| B、含有大量AlO2-的溶液:Na+、K+、NO3-、CO32- |
| C、常温下由水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+ |
| D、含有溶质为NaHSO4的溶液:K+、SiO32-、NO3-、Al3+ |
 3H2(g)+N2(g)?2NH3(g) 反应过程中的能量变化如图所示.有关说法错误的是( )
3H2(g)+N2(g)?2NH3(g) 反应过程中的能量变化如图所示.有关说法错误的是( )| A、图中C表示生成物NH3(g)的总能量 |
| B、断裂3molH-H和1mol N≡N所吸收的总能量大于形成6mol N-H所释放的总能量 |
| C、逆反应的活化能E(逆)=E+△H |
| D、3 H2(g)+N2(g)?2NH3(g)△H<0 |
下列说法正确的是( )
| A、同周期元素随核电荷数的增加,第一电离能依次增大 |
| B、元素原子的最外层电子数等于元素的最高化合价 |
| C、同主族元素从上到下,单质的熔点逐渐降低 |
| D、第ⅦA元素从上到下,其氢化物的还原性逐渐增强 |
下列叙述中,正确的是( )
| A、1 mol O2 的质量为 32 g/mol |
| B、SO42-的摩尔质量是 96 g/mol |
| C、1mol任何物质的质量等于该物质的相对分子质量 |
| D、二氧化碳的摩尔质量是44 g |
 现有8种元素,其中A、B、C、D、E为短周期主族元素,F、G、H为第4周期元素,其原子序数依次增大.请根据下列相关信息,回答问题.
现有8种元素,其中A、B、C、D、E为短周期主族元素,F、G、H为第4周期元素,其原子序数依次增大.请根据下列相关信息,回答问题.