题目内容
14.短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为13.X 的原子半径比Y 的小,X与W 同主族,Z原子的最外层电子数是内层电子数的3倍.下列说法不正确的是( )| A. | 对应的最简单氢化物的热稳定性:Z>Y | |
| B. | X、Z、W三种元素形成的化合物既含离子键,又含共价键 | |
| C. | 元素X与Y形成的化合物中,每个原子都达到了8电子稳定结构 | |
| D. | X与Z可形成既含极性共价键又含非极性共价键的化合物 |
分析 短周期元素X、Y、Z、W的原子序数依次增大,Z原子的最外层电子数是内层电子数的3倍,Z为O元素;X 的原子半径比Y 的小,X与W 同主族,则X为H,W为Na,原子最外层电子数之和为13,设Y的最外层电子数为y,则1+y+6+1=13,y=5,可知Y为N元素,然后结合元素周期律及元素化合物知识来解答.
解答 解:短周期元素X、Y、Z、W的原子序数依次增大,Z原子的最外层电子数是内层电子数的3倍,Z为O元素;X 的原子半径比Y 的小,X与W 同主族,则X为H,W为Na,原子最外层电子数之和为13,设Y的最外层电子数为y,则1+y+6+1=13,y=5,可知Y为N元素,
A.非金属性O>N,则对应的最简单氢化物的热稳定性:Z>Y,故A正确;
B.X、Z、W三种元素形成的化合物硝酸铵中既含离子键,又含共价键,故B正确;
C.元素X与Y形成的化合物水或双氧水中,O原子达到了8电子稳定结构,而H满足2电子稳定结构,故C错误;
D.X与Z可形成既含极性共价键又含非极性共价键的化合物过氧化钠,故D正确;
故选C.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构、元素的位置推断元素为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
15.下列物质中属于电解质的是( )
| A. | SO3 | B. | NaCl | C. | O2 | D. | 稀硫酸 |
5.下列叙述中,可以说明金属甲的活动性比金属乙的活动性强的是( )
| A. | 在氧化还原反应中,甲原子失去的电子比乙原子失去的电子多 | |
| B. | 同价态的阳离子,甲比乙的氧化性弱 | |
| C. | 甲不能跟稀盐酸反应放出氢气而乙能 | |
| D. | 将甲、乙作电极组成原电池时,甲是正极 |
2.2002年12月26日,俄罗斯特种部队使用强力麻醉剂芬太奴(Fentanyl)和氟烷(Halothane).下列有关氟烷(CHClBr-CF3)说法正确的是( )
| A. | 该氟烷易溶于水,也易溶于有机溶剂 | |
| B. | 该氟烷扩散到空气中能破坏臭氧层 | |
| C. | 该氟烷密度比水小 | |
| D. | 与该氟烷互为同分异构体的氟烷(不含本身)有三种 |
9.苹果酸的结构简式为 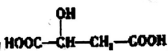 ,下列说法错误的是( )
,下列说法错误的是( )
 ,下列说法错误的是( )
,下列说法错误的是( )| A. | lmol苹果酸可与2 molNaOH发生中和反应 | |
| B. | 一定条件下,苹果酸与乙酸或乙醇均能发生酯化反应 | |
| C. |  与苹果酸互为同分异构体 与苹果酸互为同分异构体 | |
| D. | lmol苹果酸与足量金属Na反应生成1.5molH2 |
19.全国禁止在中小学幼儿园内吸烟,杜绝学生吸食“二手烟”.造成非吸烟者在公共场所吸食“二手烟”的主要原因是( )
| A. | 分子很小 | B. | 分子之间有间隙 | C. | 分子在不断运动 | D. | 分子由原子构成 |
6.A、B均为短周期主族元素,其原子的部分电离能(In,单位为kJ•mol-1)数据如表所示:
A的最高化合价为+5,基态B原子的电子排布式为1s22s22p63s23p3,A的电负性>B的电负性(填“>”、“<”或“=”).
| 序号 | I1 | I2 | I3 | I4 | I5 | I6 | I7 | |
| A的电离能 | 1402 | 2856 | 4578 | 7475 | 9445 | 53267 | … | |
| B的电离能 | 1012 | 1907 | 2914 | 4964 | 6274 | 21267 | 25431 | |
| 序号 | I8 | I9 | I10 | I11 | I12 | I13 | I14 | … |
| B的电离能 | 29872 | 35905 | 40950 | 46261 | 54110 | 59024 | 271791 | … |
3.根据有机化合物的命名原则,下列命名正确的是( )
| A. | 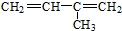 3-甲基-1,3-丁二烯 3-甲基-1,3-丁二烯 | B. | 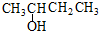 2-羟基丁烷 2-羟基丁烷 | ||
| C. | CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 | D. | CH3CH(NH2)CH2COOH 3-氨基丁酸 |
4.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 5.6 g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA | |
| B. | 1 mol Na2O2与足量H2O充分反应,转移的电子数为2NA | |
| C. | 7.8gNa2O2中含有的阴离子数等于0.1NA | |
| D. | 标况下,2.24LH2O所含分子数为0.1NA |