题目内容
现有如下两个反应:
(A)NaOH+HCl═NaCl+H2O
(B)2FeCl3+Cu═2FeCl2+CuCl2
根据两反应本质, (填A或B)能设计成原电池.如果可以则电解质溶液是 ,正极电极反应式 ,负极电极反应方程式 .
(A)NaOH+HCl═NaCl+H2O
(B)2FeCl3+Cu═2FeCl2+CuCl2
根据两反应本质,
考点:设计原电池
专题:电化学专题
分析:原电池反应必须自发进行的放热的氧化还原反应;该原电池中,失电子的金属单质作负极,不如Cu活泼的金属或导电的非金属性作正极,电解质溶液为可溶性的氯化铁溶液,负极上Cu失电子发生氧化反应、正极上铜离子得电子发生还原反应.
解答:
解:原电池反应必须自发进行的放热的氧化还原反应,A中各元素在反应前后化合价不变,所以不是氧化还原反应,则不能设计成原电池,B中为自发进行的放热的氧化还原反应,所以能设计成原电池,故选B;
该原电池中,Cu失电子作负极,不如Cu活泼的金属或导电的非金属性作正极,电解质溶液为可溶性的氯化铁溶液,正极上铜离子得电子发生还原反应,电极反应式为2Fe3++2e-=2Fe2+,负极上Cu失电子发生氧化反应,电极反应式为Cu-2e-═Cu2+,故答案为:B;FeCl3;2Fe3++2e-=2Fe2+;Cu-2e-═Cu2+.
该原电池中,Cu失电子作负极,不如Cu活泼的金属或导电的非金属性作正极,电解质溶液为可溶性的氯化铁溶液,正极上铜离子得电子发生还原反应,电极反应式为2Fe3++2e-=2Fe2+,负极上Cu失电子发生氧化反应,电极反应式为Cu-2e-═Cu2+,故答案为:B;FeCl3;2Fe3++2e-=2Fe2+;Cu-2e-═Cu2+.
点评:本题考查了原电池设计,明确原电池反应特点是解本题关键,根据方程式中元素化合价变化确定正负极,再结合发生的反应确定电解质溶液,题目难度不大.

练习册系列答案
相关题目
 如图所示装置是化学实验室中的常用装置,它有多种用途,以下各项用途和操作都正确的是( )
如图所示装置是化学实验室中的常用装置,它有多种用途,以下各项用途和操作都正确的是( )| A、洗气或干燥装置:瓶内放一定体积溶液,由a管口进气 |
| B、用于收集不溶于水的气体:瓶内充满水,由b管口进气 |
| C、提供少量CO:瓶内充满CO,b管口接自来水龙头 |
| D、H2S和SO2反应的装置:由a管口通入H2S,b管口通入SO2 |
下列说法中正确的是:①只要能源充足而且价格低廉,废弃物中的原子都可以成为有用物质的原料 ②化学家能合成大量自然界中并不存在的新物质、新材料 ③学习化学不限于书本和实验室,成功的关键在于如何激发自己对于自然现象的兴趣 ④实验是学习化学、体验化学和探究化学过程的重要途径( )
| A、③④ | B、①③④ |
| C、②③④ | D、①②③④ |
某溶液中可能存在Br-、CO32-、SO32-、Al3+、I-、Mg2+、Na+等七种离子中的几种.现取该溶液进行实验,有如下实验现象:据此可以推断,该溶液中肯定不存在的离子是( )
①向溶液中滴加足量氯水后,溶液变橙色,且有无色无味气体产生
②向所得橙色溶液中滴加足量BaCl2溶液,无沉淀生成
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.
①向溶液中滴加足量氯水后,溶液变橙色,且有无色无味气体产生
②向所得橙色溶液中滴加足量BaCl2溶液,无沉淀生成
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.
| A、Mg2+、Na+、CO32-、I- |
| B、Al3+、Na+、SO32-、I- |
| C、Al3+、Mg2+、SO32-、I- |
| D、Al3+、CO32-、Br-、SO32- |
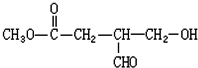
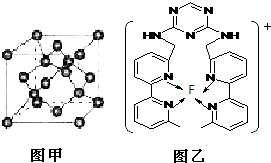 现有A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期.A元素能级个数与核外电子数相等,B元素含有3个能级,且每个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子.请回答下列问题:
现有A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期.A元素能级个数与核外电子数相等,B元素含有3个能级,且每个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子.请回答下列问题: