题目内容
8. 甲同学向做过银镜反应的试管0.1mol/L的Fe(NO3)3溶液(pH=2),发现银镜部分溶解,和大家一起分析原因:
甲同学向做过银镜反应的试管0.1mol/L的Fe(NO3)3溶液(pH=2),发现银镜部分溶解,和大家一起分析原因:甲同学认为:Fe3+具有氧化性,能够溶解单质Ag
乙同学认为:Fe(NO3)3溶液显酸性,该条件下NO3-也能氧化单质Ag.
丙同学认为:Fe3+和NO3-均能把Ag氧化而溶解.
(1)生成银镜反应过程中银氨溶液发生还原 (氧化、还原)反应.
(2)为得出正确结论,只需设计两个实验验证即可.
实验Ⅰ:向溶解了银镜的Fe(NO3)3的溶液中加入②(填序号,①KSCN溶液、②K3[Fe(CN)6]溶液、③稀HCl),现象为产生蓝色沉淀,证明甲的结论正确.
实验Ⅱ:向附有银镜的试管中加入pH=2的 0.3 mol/L KNO3或NaNO3 溶液,观察银镜是否溶解.
两个实验结果证明了丙同学的结论
(3)丙同学又把5mlFeSO4溶液分成两份:
第一份滴加2滴KSCN溶液无变化;第二份加入1ml 0.1mol/L AgNO3溶液,出现白色沉淀,随后有黑色固体产生(经验证黑色固体为Ag颗粒),再取上层溶液滴加KSCN溶液变红.根据上述的实验情况,用离子方程式表示Fe3+、Fe2+、Ag+、Ag之间的反应关系Fe3++Ag?Fe2++Ag+或Ag++Fe2+?Ag+Fe3+.
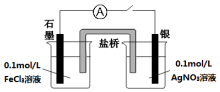
(4)丁同学改用如图实验装置做进一步探究:
①K刚闭合时,指针向左偏转,此时石墨作正极,(填“正极”或“负极”).此过程氧化性:Fe3+> Ag+(填“>”或“<”).
②当指针归零后,向右烧杯中滴加几滴饱和AgNO3溶液,指针向右偏转.
此过程氧化性:Fe3+< Ag+(填“>”或“<”).
由①和②的实验,得出的结论是:在其它条件不变时,物质的氧化性与浓度有关,浓度的改变可导致平衡移动.
分析 (1)银氨溶液中的银为+1价,被醛基还原生成0价的银单质;
(2)实验Ⅰ:亚铁离子的检验是K3[Fe(CN)6]溶液和亚铁离子结合生成蓝色沉淀,据此进行解答;
实验Ⅱ:硝酸根离子也可能氧化单质银,需进行对照实验,配制同PH、同硝酸根离子浓度的溶液进行对照;
(3)第一份滴加2滴KSCN溶液无变化,无铁离子,第二份加入1ml 0.1mol/L AgNO3溶液,出现白色沉淀,随后有黑色固体产生,经验证黑色固体为Ag,再取上层溶液滴加KSCN溶液变红,存在铁离子,说明铁离子氧化银生成亚铁离子,该反应为可逆反应;
(4)①原电池负极发生氧化反应,正极发生还原反应,氧化还原反应中氧化剂的氧化性大于氧化产物;
②当指针归零后,向右烧杯中滴加几滴饱和AgNO3溶液,指针向右偏转,说明主要发生Ag++Fe2+?Ag+Fe3+;增大反应物的浓度,平衡移动,说明物质的氧化性与浓度有关,浓度的改变可导致平衡移动.
解答 解:(1)往AgNO3溶液中逐滴加入氨水,银离子和氨水反应生成白色的氢氧化银沉淀和铵根离子,离子反应方程式为:Ag++NH3•H2O═AgOH↓+NH4+;继续滴入氨水白色沉淀溶解,氢氧化银和氨水反应生成银氨溶液和水,离子反应方程式为:AgOH+2NH3•H2O═[Ag(NH3)2]OH+2H2O,若用乙醛进行银镜反应,再加入乙醛溶液后,生成乙酸铵,氨气、银和水,化学反应方程式为:CH3CHO+2Ag(NH3)2OH$\stackrel{水浴}{→}$CH3COONH4+2Ag↓+3NH3+H2O,银氨溶液中的银为+1价,被醛基还原生成0价的银单质,
故答案为:还原;
(2)实验Ⅰ:验证亚铁离子实验是取少量除尽Ag+后的溶液于试管中,加入K3[Fe(CN)6]溶液会和亚铁离子反应生成蓝色沉淀,
故答案为:②;产生蓝色沉淀;
实验Ⅱ:硝酸根离子也可能氧化单质银,需进行对照实验,0.1mol/L的Fe(NO3)3溶液(pH=2),硝酸根离子为0.3 mol/L,所以需向附有银镜的试管中加入pH=2的 0.3 mol/L KNO3或NaNO3溶液,
故答案为:pH=2的 0.3 mol/L KNO3或NaNO3;
(3)Fe3+与SCN-反应生成红色的硫氰化铁溶液,Fe3++3SCN-?Fe(SCN)3,呈红色,第一份滴加2滴KSCN溶液无变化,无铁离子,第二份加入1ml 0.1mol/L AgNO3溶液,出现白色沉淀,随后有黑色固体产生,经验证黑色固体为Ag,再取上层溶液滴加KSCN溶液变红,存在铁离子,说明铁离子氧化银生成亚铁离子,且该反应为可逆反应,所以反应为:Fe3++Ag?Fe2++Ag+或Ag++Fe2+?Ag+Fe3+,
故答案为:Fe3++Ag?Fe2++Ag+或Ag++Fe2+?Ag+Fe3+;
(4)①该电池的反应本质为Fe3++Ag?Fe2++Ag+,银为负极,石墨为正极,该反应中铁离子为氧化剂,银离子为氧化产物,所以此过程氧化性:Fe3+>Ag+,
故答案为:正极;>;
②当指针归零后,向右烧杯中滴加几滴饱和AgNO3溶液,Fe3++Ag?Fe2++Ag+,银离子浓度增大,平衡右移,主要反应为:Ag++Fe2+?Ag+Fe3+,
氧化还原反应中氧化剂的氧化性大于氧化产物,所以此过程氧化性:Fe3+<Ag+,由①和②的实验,得出的结论是:在其它条件不变时,物质的氧化性与浓度有关,浓度的改变可导致平衡移动,
故答案为:<;在其它条件不变时,物质的氧化性与浓度有关,浓度的改变可导致平衡移动.
点评 本题为探究实验,考查实验操作、物质的检验等知识,题目难度中等,注意掌握实验设计的方法和物质实验验证方案分析方法,侧重考查了学生提出假设并设计实验验证的能力、分析问题解决问题的能力及提取信息的能力,题目难度中等.

| A. | 混合气体的压强 | B. | 气体的总体积 | ||
| C. | 混合气体的相对分子质量 | D. | 气体的总物质的量 |
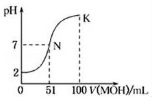 常温下,向100mL 0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1的MOH溶液,图中所示曲线表示混合溶液的pH变化情况,下列说法不正确的是( )
常温下,向100mL 0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1的MOH溶液,图中所示曲线表示混合溶液的pH变化情况,下列说法不正确的是( )| A. | HA为一元强酸,MOH为一元弱碱 | |
| B. | N点溶液中离子浓度大小关系为:c(M+)=c(A-)>c(H+)=c(OH-) | |
| C. | N点水的电离程度大于K点水的电离程度 | |
| D. | N→k之间曲线上任意一点都有c(M+)>c(OH-)>c(A-)>c(H+) |
| A. | 盛放碱液的试剂瓶不用玻璃塞;SiO2+2OH-═SiO32-+H2O | |
| B. | 配制FeCl3溶液时要加盐酸:Fe3++3H2O?Fe(OH)3+3H+ | |
| C. | 制Cl2时用排饱和氯化钠溶液收集气体:H2O+Cl2?Cl-+H++HClO | |
| D. | 金属钠燃烧时,火焰呈黄色:2Na+O2 $\frac{\underline{\;点燃\;}}{\;}$Na2O2 |
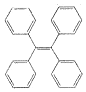 TPE及其衍生物具有诱导发光特性,在光电材料等领域应用前景广泛.TPE的结构简式如图,下列关于TPE的说法正确的是( )
TPE及其衍生物具有诱导发光特性,在光电材料等领域应用前景广泛.TPE的结构简式如图,下列关于TPE的说法正确的是( )| A. | TPE属于苯的同系物 | |
| B. | TPE能发生加成反应,但不能取代反应 | |
| C. | TPE与化合物 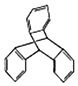 互为同分异构体 互为同分异构体 | |
| D. | TPE的一氯代物有3种 |
| 实验内容 | 实验现象 | 相关解释 | |
| A | 等量的Cu分别与等体积足量的浓硝酸和稀硝酸反应 | 浓硝酸反应后呈绿色,稀硝酸反应后呈蓝色 | c(Cu2+)不同 |
| B | NH3与Cl2混合 | 生成白烟 | NH3与Cl2发生化合反应生成NH4Cl |
| C | 往Fe(OH)3胶体中逐滴滴入稀盐酸 | 先出现红褐色沉淀,后沉淀溶解 | 先胶体聚沉,后Fe(OH)3溶解 |
| D | 加热硝酸铜固体,将带火星的木条伸入所得的气体中 | 生成红棕色气体,带火星木条复燃 | 2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+4NO2↑+O2↑有氧气生成,不能说明NO2有助燃性. |
| A. | A | B. | B | C. | C | D. | D |
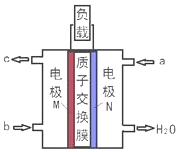 甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用.某型甲醇燃料电池的总反应式2CH4O+3O2═2CO2+4H2O,下图是该燃料电池的示意图.下列说法正确的是( )
甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用.某型甲醇燃料电池的总反应式2CH4O+3O2═2CO2+4H2O,下图是该燃料电池的示意图.下列说法正确的是( )| A. | a是甲醇燃料、b是氧气 | |
| B. | 当转移6mol e-时,消耗33.6L O2 | |
| C. | 负极反应:CH4O-6e-+H2O═CO2↑+6H+ | |
| D. | 质子从N电极区穿过交换膜移向M电极区 |
| A. | 苯乙烯 | B. | 乙烯 | C. | 乙醇 | D. | 聚乙烯 |