题目内容
6.在无色溶液中,下列各组离子能大量共存的是( )| A. | K+、SO42-、Cl-、NH4+ | B. | Na+、NO3-、Ag+、CO32- | ||
| C. | Na+、Cl-、NO3-、Cu2+、 | D. | K+、HCO3-、SO42-、OH |
分析 溶液无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,
A.四种离子之间不反应,都是无色离子;
B.银离子与碳酸根离子反应生成碳酸银沉淀;
C.铜离子为有色离子;
D.碳酸氢根离子与氢氧根离子反应.
解答 解:无色溶液时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,
A.K+、SO42-、Cl-、NH4+之间不发生反应,为无色溶液,在溶液中能够大量共存,故A正确;
B.Ag+、CO32-之间反应生成难溶物碳酸银,在溶液中不能大量共存,故B错误;
C.Cu2+为有色离子,不满足溶液无色的要求,故C错误;
D.HCO3-、OH-之间发生反应,在溶液中不能大量共存,故D错误;
故选A.
点评 本题考查离子共存的判断,为高考的高频题,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
16.下列说法正确的是( )
| A. | 能电离出H+的化合物叫做酸 | |
| B. | 摩尔是七个基本物理量之一 | |
| C. | 化合物分为酸、碱、盐和氧化物是用树状分类法分类的 | |
| D. | 实验测得1mol某气体体积为22.4L,测定条件一定是标准状况 |
17. 在一定条件下,在容积不变的密闭容器内进行反应:2NO+2CO?N2+2CO2 △H<0.曲线a表示NO的转化率与反应时间的关系,若改变初始条件,使反应过程按照曲线b进行,可采取的措施是( )
在一定条件下,在容积不变的密闭容器内进行反应:2NO+2CO?N2+2CO2 △H<0.曲线a表示NO的转化率与反应时间的关系,若改变初始条件,使反应过程按照曲线b进行,可采取的措施是( )
 在一定条件下,在容积不变的密闭容器内进行反应:2NO+2CO?N2+2CO2 △H<0.曲线a表示NO的转化率与反应时间的关系,若改变初始条件,使反应过程按照曲线b进行,可采取的措施是( )
在一定条件下,在容积不变的密闭容器内进行反应:2NO+2CO?N2+2CO2 △H<0.曲线a表示NO的转化率与反应时间的关系,若改变初始条件,使反应过程按照曲线b进行,可采取的措施是( )| A. | 加催化剂 | B. | 降低温度 | C. | 增大NO的浓度 | D. | 缩小容器体积 |
14.下列有关氯气及其化合物的说法不正确的是( )
| A. | 氯气能与大多数金属化合,其一般将变价金属氧化至最高价 | |
| B. | 干燥的氯气和氯水均能使鲜花褪色 | |
| C. | 除去氯气中少量氯化氢可使气体通过饱和食盐水 | |
| D. | 因为氯气有毒,所以可用于杀菌、消毒、漂白 |
1.在配制一定物质的量浓度的NaOH溶液时,下列说法正确的是( )
| A. | 将称量NaOH固体时在烧杯中溶解后立即转移到容量瓶中 | |
| B. | 向容量瓶中加水定容时俯视 所配溶液浓度偏高 | |
| C. | 配制NaOH溶液不需用到量筒 | |
| D. | 定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线 |
18.下列有关物质分类说法正确的是( )
| A. | 纯碱、液态氧、碘酒、稀盐酸依次是盐、单质、混合物、电解质 | |
| B. | 干冰、生石灰、硫酸、碳酸氢铵依次是单质、氧化物、酸、盐 | |
| C. | 氯化氢、氨气、水银、草木灰依次是电解质、非电解质、单质、混合物 | |
| D. | 冰水、空气、泥水依次是溶液、胶体、浊液 |
15.某混合气体中可能含有Cl2、O2、SO2、NO、NO2 中的两种或多种气体.现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色.对于原混合气体成分的判断中正确的是( )
| A. | 肯定有SO2 和NO | B. | 肯定有SO2和NO2 | ||
| C. | 可能有Cl2、NO和O2 | D. | 肯定有SO2、NO和O2 |
9.常温下,用0.10mol•L-1的HCl溶液滴定20.00mol•L-1氨水,滴定曲线如图.下列说法正确的是( )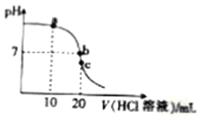

| A. | a点对应的溶液中,c(Cl-)>c(NH4+ )>c(OH- )>c(H+ ) | |
| B. | b点对应的溶液中,c(NH4+)>c(Cl-),c(OH- )=c(H+ ) | |
| C. | c点对应的溶液中,c(H+)=c(NH3•H2O)+c(OH- ) | |
| D. | 滴定过程中可能出现:c(NH4+ )>c(OH- )>c(H+ )>c(Cl-) |
 .
.