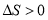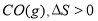题目内容
25°C时,水的电离达到平衡:H2O H++OH-,下列叙述正确的是( )
H++OH-,下列叙述正确的是( )
A.将纯水加热到950C时,Kw变大,pH不变,水仍呈中性
B.向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,Kw变小
C.向纯水中加人少量固体碳酸钠,c(H+)减小,Kw不变,促进水的电离
D.向纯水中加入醋酸钠或盐酸,均可抑制水的电离,Kw不变
C
【解析】
试题分析:A.将纯水加热到950C时,Kw变大,pH应该减小,水仍呈中性,错误;B.向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,Kw应该不变,错误;C.向纯水中加人少量固体碳酸钠,c(H+)减小,Kw不变,促进水的电离,正确;D.向纯水中加入醋酸钠促进了水的电离,而加入盐酸抑制水的电离,Kw不变,错误;
考点:本题考查水的电离平衡移动,从浓度、温度对平衡移动的影响角度分析,本题易错点为C,注意升高温度c(H+),pH减小。

现有A、B、C、D、E五种可溶强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
阳离子 | H+、Na+、Al3+、Ag+、Ba2+ |
阴离子 | OH-、Cl-、CO32-、NO3-、SO42- |
已知:①A、B两溶液呈碱性; C、D、E溶液呈酸性。
②向E溶液中逐滴滴加B溶液至过量,沉淀量先增加后减少但不消失。
③D溶液与另外四种溶液反应都能产生沉淀。
试回答下列问题:
(1)A溶液呈碱性的原因是 (用离子方程式表示)。
(2)写出E溶液与过量的B溶液反应的离子方程式 。
(3)若25°时C、E溶液pH=4,则E溶液中水电离出的氢离子浓度是C溶液中水电离出的氢离子
浓度 倍。
(4)将C溶液逐滴加入等体积、等物质的量的浓度的A溶液中,反应后溶液中一价离子(+1或-1)
浓度由大到小的顺序为: 。